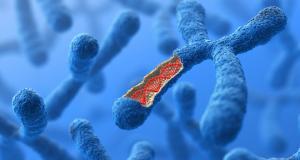
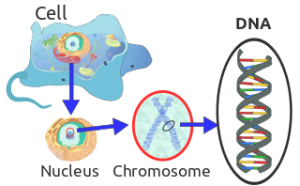
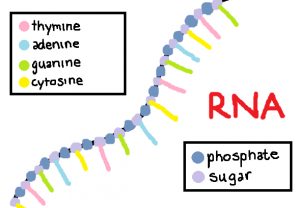
 DNA’da bulunan genler, dış görünüşü ve vücut işlevlerini kodladıkları proteinler aracılığıyla etkilerler. Kodlama işlevi ise genlerin proteinin nasıl sentezleneceğine dair bilgiyi yani DNA dizisini taşıdığını ifade eder. DNA’nın yapısı dört tane nükleotit adı verilen alt birimlerden oluşur ve bu dört farklı nükleotidin farklı kombinasyonlarda dizilmesi ise farklı dizileri oluşturur. Bu nedenle de farklı genler farklı diziler içerir ve farklı genlerden çeşitli proteinler sentezlenir. Bir protein sentezlenirken ise, gendeki diziye uyumlu bir mRNA molekülü sentezlenir ve mRNA hücrede protein sentezinden sorumlu ribozom adı verilen organele giderek protein sentezinin gerçekleşmesini sağlar. Bu sürece bazen, mRNA’dan farklı olan ve protein kodlamayan bazı RNA türleri dahil olur ve mRNA’nın dizisine bağlanarak ilgili proteinin sentezlenmesini önleyebilir.
DNA’da bulunan genler, dış görünüşü ve vücut işlevlerini kodladıkları proteinler aracılığıyla etkilerler. Kodlama işlevi ise genlerin proteinin nasıl sentezleneceğine dair bilgiyi yani DNA dizisini taşıdığını ifade eder. DNA’nın yapısı dört tane nükleotit adı verilen alt birimlerden oluşur ve bu dört farklı nükleotidin farklı kombinasyonlarda dizilmesi ise farklı dizileri oluşturur. Bu nedenle de farklı genler farklı diziler içerir ve farklı genlerden çeşitli proteinler sentezlenir. Bir protein sentezlenirken ise, gendeki diziye uyumlu bir mRNA molekülü sentezlenir ve mRNA hücrede protein sentezinden sorumlu ribozom adı verilen organele giderek protein sentezinin gerçekleşmesini sağlar. Bu sürece bazen, mRNA’dan farklı olan ve protein kodlamayan bazı RNA türleri dahil olur ve mRNA’nın dizisine bağlanarak ilgili proteinin sentezlenmesini önleyebilir.
İnsan genomunda en ayrıntılı çalışılmış kısımlar protein kodlamayan dizilerdir. Buna rağmen, protein kodlayan kısmlar genomun sadece %1,5’unu oluşturur. Son yıllarda protein kodlayaman kısımların normal gelişim, fizyoloji ve hastalıklar için önemli olduğu ortaya çıkmıştır. Protein kodlamayan genomun fonksiyonal ilişkisi, mikroRNA adı verilen küçük kodlama yapmayan RNA’ların varlığı ile kanıtlandı. Özellikle kanser gibi insan hastalıklarında, miRNA ve mekanizmasındaki genetik hastalıkların yaygın ayırıcı özelliğidir. Buna rağmen miRNA’lar buz dağının sadece görünen kısmıdır. Diğer türde kodlama yapmayan RNA’lar da insan hastalıklarının gelişimine neden olabilir.
 miRNA’lar
miRNA’lar
miRNA’ların uzunluğu 22 nükleotitten kısadır. Hayvanlarda mRNA’nın protein kodlamasını önlemek için mRNA’ya bağlanır. miRNA’ların protein kodlayan genlerin %60’ından fazlasının aktivitesini düzenlediği düşünülüyor. Çoğalma, farklılaşma, apoptoz (hücre ölümü) ve gelişim dahil çok sayıda sürecin düzenlenmesiyle ilişkilidirler. Bazı miRNA’lar sadece tek bir hedefle ilişkiliyken, bazıları tüm bir süreci yönetebilir. Bu nedenle birden fazla genin aktivitesini eş zamanlı olarak yöneten miRNA’lar vardır. miRNA’nın üretilmesi çok aşamalı bir süreçtir. Bu sürece Rnase enzimi olan Drosha ve Dicer dahildir ve süreç 22 nükleotid uzunluğunda bir miRNA’nın üretilmesiyle sona erer. Bu moleküller Dicer-TARBP2 adlı bir proteine bağlanır ve Argonaute proteiniyle birlikte RISC kompleksini oluşturur. RISC kompleksindeki argonat katalitik nükleik asit parçalayan bir bileşendir ve miRNA mRNA’ya bağlandığında mRNA’yı parçalar. mRNA’ların proteini kodlaması işlevi miRNA’lar tarafından ya mRNA’nın parçalanmasıyla ya da protein sentezinin başlamasının engellenmesiyle durdurulur.
piRNA’lar
piRNA’lar 24-34 nükleotit uzunluğundadır. Dicer’dan bağısızdırlar ve argonat ailesinin bir üyesi olan PIWI adlı bir proteine bağlanırlar. Bu RNA türü üreme hücrelerinde genomun yapısının stabilliğini sağlar. Genomda transpozonların ve diğer tekrarlı dizilerin olduğu yerlerden sentezlenirler. piRNA ve PIWI proteinleri kompleksi genomda hareketli olan transpozon adlı dizilerin aktivitesini ve hareketini baskılar. mRNA baskılanması ile ilişkisi yoktur. Genomda belli bölgelerin aktivitesini metil grubu ekleme mekanizmasıyla sınırlar.
snoRNA’lar
snoRNA’lar 60-300 nükleotit büyüklüğünde RNA’lardır. Bazı küçük proteinlerle birarada bulunur. Bu yapı, ribozomun yapısında bulunan RNA’nın dizisine özel metil grubu eklenmesinden sorumludur. SnoRNA’nın varlığı bu işlemin diziye özgü olmasını sağlar.
l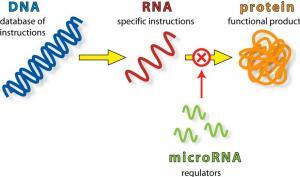 ncRNA’lar
ncRNA’lar
200 nükleotitten uzundurdurlar ve çok sayıda biyolojik süreçle ilişkilidirler. Memeli hücrelerinde yüksek oranda bulunurlar. Memelilerde cinsiyet kromozomları (DNA’nın proteinlerle sıkıca paketlenmiş hali) dişilerde XX ve erkeklerde XY şeklindedir. Dişilerde bulunan iki X kromozomundan birinin aktivitesi baskılanmıştır. LncRNA’lar da bu X kromozomunun inaktivasyonunda görevlidir. Bu gruba ait RNA türlerinden biri de lincRNA’dır ve bu RNA türü DNA hasarına cevap veren genlerin aktivitesini baskılar.
Telomerlerin (kromozomların ucununda bulunan ve kromozomların yapısal bütünlüğünü koruyan dizi) kodladığı bir RNA olan TERRA’da telomeraz aktivitesini düzenleyerek telomerlerin bütünlüğünü sağlar.
RNA’ların Kanserle İlişkisi
İnsan kanserlerinde, normal doku ile tümör dokusunda bulunan miRNA profili açısından fark vardır. miRNA’lar onkogen (kanserlerde kontrolsüz hücre çoğalmasına neden olan genler) ya da tümör baskılayıcı genler (kontrolsüz hücre çoğalmasını engelleyen genler) gibi davranarak tümör gelişiminde anahtar rol oynayabilir. miRNA’yı kodlayan genlerde metilasyon gibi epigenetik değişiklikler olması ve genetik değişiklikler olması sonucunda bazı kanser türlerinde miRNA fonksiyon bozukluğu görülebilir. miRNA ve kanser ilişkisi ilk defa lösemide 13.kromozomda parça kaybı sonucu miR-15 ve miR-16 adllı miRNA’lardaki fonksiyon bozukluğu olarak görüldü. İlginç şekilde miRNA’lar genomun kırılmaya yatkın bölgelerinde bulunur ve yumurtalık, meme ve cilt kanserleriyle ilişkidirler.
piRNA’ların Kanserle İlişkisi
Tümör oluşumundaki işlevleri bilinmemesine rağmen, piRNA’ların testis kanseriyle ve birçok kanser türüyle ilişkisi tespit edildi. piRNA’ların meknizmasıyla ilişkili olan PIWI proteinlerinin çeşitli tümörlerde normalden fazla miktarda olduğu gözlemlendi. Daha sonraki çalışmalar ise insan kanser hücresi modelinde PIWIL1 proteinin hücre döngüsünün durmasında ve PIWIL2 proteininin ise hücre çoğalması ve anti-apoptotik (hücre ölümüne karşı) sinyale neden olduğunu gösterdi.
PiRNA ve PIWI proteinlerinin kanser yapıcı etkilerinin altında yatan mekanizma tam olarak bilinmese de ilişkili oldukları birkaç mekanizma bilinmektedir. PIWI proteinleri kök hücre çoğalmasıyla da ilişkilidir ve tümöre dönüşme potansiyeli olan kansere dönüşmemiş hücrede tekrar sentezlenir.
 RNA’ların Nörolojik Hastalıklarla İlişkisi
RNA’ların Nörolojik Hastalıklarla İlişkisi
Çok sayıda rollerinin yanısıra miRNA’ların sinir sisteminde de önemli görevleri vardır. İnsan vücudundaki miRNA’ların %70’i beyinde sentezlenir ve bunların çoğu nöronlara özgüdür. Bu miRNA’ların sinirsel gelişimde rolü vardır ve işlevlerindeki bozukluklar nörolojik hastalıklarda gözlemlenmiştir. Örneğin; miR-206 eksikliği ALS’nin (bir motor nöron hastalığı) ilerleyişini hızlandırır. Alzheimer hastalığında ise, anormal şekilde üretilen bir miRNA, BACE1 isimli enzimin üretimini baskılar. Bu durum da Alzheimer belirtilerine neden olan beta-amiloid proteinin beyin dokusunda birikmesine neden olur. Benzer şekilde Parkinson hastalığında da bir miRNA, alfa-sinüklein proteinin birikimini kontrol eder.
RNA’ları Hedefleyen Terapiler
Protein kodlamayan RNA’lar ve ilişkili oldukları proteinler, yeni terapi stratejilerinin hedefleridir. Bu stratejilerden biri de miRNA’nın işlevini baskılamaktır.
miRNA’lar hedeflerini nükleotit dizilerine bağlanarak etkisiz hale getirirler. miRNA’ları etkisiz hale getirmek için ise, miRNA dizisine tamamlayıcı şekilde diziye sahip kısa bie nükleotit dizisi olan antisense oligonükleotitlerden (ASO) yararlanılır.
ASO terapisinin etkisi birkaç uygulamada gösterildi. Fare kanser modelinde miR-10b’yi hedefleyen bir ASO’nun verilmesi kanserin metaztazını önledi. Kardiyovasküler hastalıklar için de, miR-122’yi hedefleyen ASO’nun sistemik olarak vücuda verilmesi plazmadaki kolesterol seviyesini düşürdü.
Yapılan başarılı çalışmalara rağmen, tek bir miRNA’nın inhibe edilmesi yeterli olmayabilir. Çünkü çoğu hastalığın, özellikle de kanserin oluşumunu etkileyen birden fazla molekül ve mekanizma vardır. Bu nedenle yapılan son araştırmalarda birden fazla miRNA’ya eş zamanlı bağlanabilen tek bir ASO geliştirildi. Gelecek çalışmalarda geliştirilen bu ASO, birden fazla miRNA’yı inhibe ederek, kanser hücrelerinin kontrolsüz çoğalmasını, metastazı ve anjiogenezi eş zamanlı durudurabilir.
Şimdiye kadar RNA’lara yönelik uygulanan terapi stratejileri sadece laboratuvarda hücreler ve fare modelleri üzerinde denenmiştir. Bu nedenle bu tedavi yöntemlerinin etkinliğinin kanıtlanması için klinikte hastalar üzerinde çalışma yapılmasına da ihtiyaç vardır. RNA’lara yönelik terapiler henüz oldukça yeni bir alan olmasına rağmen, gelecekteki çalışmalar açısından umut vericidir.
Kaynakça:
Esteller. Non-coding RNAs in human diseases. Nature Genetics (2011).
Yazar: Ayça Olcay
