 Kanser tedavileri yıllarca; ameliyat, kemoterapi ve radyasyon terapisine dayalıydı. İmatinib ve trastuzumab gibi ilaçlar ise sadece kanser hücrelerini hedef alır. Son yıllarda gelişen immünoterapi yaklaşımı adaptive edici hücre transferi (ACT ) adını alır. Hastanın kendi bağışıklık sistemi hücreleri, kanseri tedavi etmek için kullanır. ACT’nin birkaç türü vardır ama bu türlerden sadece CAR T hücre terapisi klinik faza ulaşabilmiştir.
Kanser tedavileri yıllarca; ameliyat, kemoterapi ve radyasyon terapisine dayalıydı. İmatinib ve trastuzumab gibi ilaçlar ise sadece kanser hücrelerini hedef alır. Son yıllarda gelişen immünoterapi yaklaşımı adaptive edici hücre transferi (ACT ) adını alır. Hastanın kendi bağışıklık sistemi hücreleri, kanseri tedavi etmek için kullanır. ACT’nin birkaç türü vardır ama bu türlerden sadece CAR T hücre terapisi klinik faza ulaşabilmiştir.
Şu ana kadar CAR T hücre terapisinin kullanımı, ileri derecede kan kanseri olan hastalarda kullanılmak üzere küçük klinik denemelerle sınırlandırıldı. Fakat bu tedaviler araştırmacıların dikkatini çekti. Çünkü bu terapi ile tedavi olan yetişkinlerde ve çocuklarda belirgin bir ilerleme gözlemlendi.
2017 yılında iki CAR T hücre terapisi FDA tarafından onaylandı. Bunlardan biri çocuklarda akut lenfoblastik lösemi (ALL) tedavisidir ve diğeri yetişkinler için ileri lenfomadır. Yine de araştırmacılar, CAR T hücre terapilerinin erken evrede olduğunu söylüyorlar. Bu terapi türünün meme ve kolon kanseri gibi solid tümörler üzerine etkili olup olmadığı henüz bilinmiyor.
ACT’nin farklı formları hala gelişme aşamasındadır. Fakat yıllarca yapılan özenli çalışmaların ardından, durağan noktaya gelindi. Geçtiğimiz birkaç yılda CaR T hücre terapisi ve diğer ACT yaklaşımları hızlı şekilde arttı. Araştırmacılar bu terapilerin hastalarda nasıl çalıştığı ve nasıl gelişeceği ve test edileceği ile ilgili ilerleme kaydetti. Önümüzdeki birkaç yılda ise bu tür terapiler hızla yaygınlaşacaktır.
Yaşayan İlaç
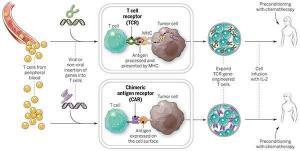
CAR T hücre terapisinin bel kemiğini, bağışıklık sistemi cevabını aktive eden ve enfekte olan hücreleri öldüren T hücreleri oluşturur. Bu terapide hastanın kanı alınır ve T hücreleri ayrılır. Sonraki aşamada zararsız bir virüs kullanılarak T hücreleri genetik mühendisliği yöntemiyle modifiye edilir ve yüzeyinde kimerik antijen reseptörü adı verilen CAR reseptörlerini üretir. Bu reseptörler, doğal olarak var olmayan sentetik moleküllerdir.
Özel reseptörler, T hücrelerinin özgül bir proteini tanıyıp, yok edeceği hücreye bağlanmalarını sağlar. CAR T hücre terapileri, B hücrelerindeki CD19 antijenini (proteinini) hedef alır. T hücreleri toplandığında antijene özgü CAR üretir ve laboratuvarda milyonlarca hücre olarak üretilir.
Son aşama, CAR T hücrelerinin hastaya aktarılmasıdır. Planlandığı gibi olursa T hücreleri, hastanın vücudunda çoğalmaya devam edecektir ve sentetik reseptörün rehberliğiyle kanser hücrelerini öldürecektir.
Çok sayıda CAR T hücre terapisi klinik çalışmalar için geliştirilmekte ve test edilmektedir. Terapi türleri arasında farklılıklar olsa da benzer bileşenleri taşırlar. Hücre yüzeyindeki CAR, sentetik antikorların fragmentlerinden ya da domenlerinden (parçalarından) oluşur. Kullanılan domenler, tümör hücresindeki antijeni reseptörün ne kadar iyi tanıdığını ya da bağlandığını etkiler.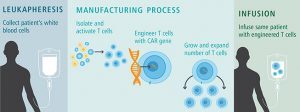
CAR T hücre terapisinin başlagıçtaki gelişimi, çocuklardaki en yaygın kanser türü olan ALL üzerine odaklanmıştır. B hücrelerinden ortaya çıkan ALL tanısı koyulan çocukların %80’i, yoğun kemoterapi ile tedavi ediliyordu. Fakat kök hücre transplantasyonundan ya da kemoterapiden sonra tekrarlayan kanser için tedavi seçeneği neredeyse yoktu. Tekrarlayan ALL ise, çocukluk çağı kanserlerinde en yaygın görülen ölüm nedeniydi.
Dr. Grupp, kanseri tekrarlayan ya da var olan terapilere cevap vermeyen ALL hastası olan genç yetişkinlerde ve çocuklarda, CAR T hücreleriyle birkaç deneme yaptı. Başlangıç denemelerinden birinde, CD19 reseptörlerine bağlanan CAR T hücreleri kullanıldı. 30 hastanın 27’sinde tüm kanser belirtileri kayboldu. Tedaviden sonra hastaların çoğunda kanser tekrarlamadı.
Kymriah adı verilen CD19 hedefli CAR T hücre terapisi için çocuklarda ve gençlerde, başlangıçtaki başarının ardından daha geniş çaplı terapi yapıldı. Terapiye katılan pek çok hasta uzun süreli iyileşme gösterdi. Bunun sonucunda, Ağustos 2017’de FDA ilacı onayladı.
Fakat buna karşın, kan kanseri olan genç yetişkinlerin tedavisi için CAR T hücre terapisi ile ilgili umut verici bir sonuca ulaşılmadı. C19 hedefli CAR T hücre terapisi, ALL’nin yanısıra lenfoma hastaları için de iyi sonuçlar gösterdi.
Yan Etkilerle Başa Çıkmak
Tüm kanser terapilerinde olduğu gibi bu terapide de ciddi ve hata ölüme neden olabilecek yan etkiler görülebilir. En sık görüleni ise, sitokin salınım sendromudur (CRS). Bağışıklık sistemi ile ilgli işlerin bir parçası olarak, T hücreleri sitokin (bağışıklık sistemi cevabını uyaran kimyasallardır) salgılar. CRS durumunda hızlıca çok miktarda sitokin kan akışına salınır ve bu da yüksek ateşe ve kan basıncında hızlı düşüşe neden olur.
Aynı zamanda CRS’nin ortaya çıkışı, aktif T hücrelerinin vücutta çalıştığını gösterir. Genellikle CAR T tedavisinden önce daha ağır şekilde hasta olan kişiler CRS tecrübe etme eğilimindeler. Çok sayıda hastada CRS, steroid verilerek tedavi edilebilir. Birkaç yıl önce ciddi derede CRS tecrübe eden hastalarda, iltihaba karşı T hücrelerinden ve makrofajlardan salınan yüksek seviyede IL-6 sitokini gözlemlediler. Artrit tedavisinden olduğu gibi IL-6’yı bloklayan ilaçların kullanılması hastalarda CRS’yi tedavi etti. Bu nedenle, bu tür tedavi CRS için standart hale geldi.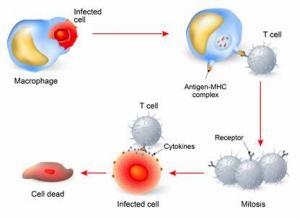
CAR T hücre terapisinin diğer bir yan etkisi, B hücrelerinin yüksek oranda ölmesidir. Normal B hücrelerinde CD19 antijeni, antikor üretmekle sorumludur. Normal B hücreleri ise CAR T hücreleri tarafından öldürülür. Bu hasarı telafi etmek için hastanın immünoglobulin terapisi alması gerekir.
CAR T hücre terapisinin geliştirilmesine yönelik çalışmalar devam etmektedir. Bu çalışmalardan bazıları; nanoteknoloji kullanarak CAR T hücrelerinin vücudun içerisinde geliştirilmesi ve CRS’ye benzer yan etkilerin oluşmaması için yapılan çalışmalardır. Var olan CAR T terapi yönteminin geliştirilmesi için yapılacak daha çok çalışma vardır.
Kaynakça:
https://www.cancer.gov/about-cancer/treatment/research/car-t-cells
Yazar: Ayça Olcay
