 Enzimlerin, yaşam kimyasındaki seçici katalizleme molekülleridir. Biyolojik tepkimelerin termodinamiği konusunda sık sık bahsedilen katalizör çoğunlukla enzim olmaktadır. Serbest enerji salan bir kimyasal tepkime kendiliğinden gerçekleşebilir. Gerekli aktivasyon enerjisi oldukça yüksek olduğundan, biyokimyasal tepkimeler katalizör katılmadığında son derece yavaş gelişirler. Katalizörler, enzimler de dahil olmak üzere, ne tepkimenin denge sabitini, ne de serbest enerjideki net değişimi etkilerler. Kendi başlarına, bir tepkimenin yukarı doğru olmasını sağlayamazlar, ama aşağı doğru ilerleyen belirli tepkimelerin çok daha hızlı gerçekleşmesini sağlarlar.
Enzimlerin, yaşam kimyasındaki seçici katalizleme molekülleridir. Biyolojik tepkimelerin termodinamiği konusunda sık sık bahsedilen katalizör çoğunlukla enzim olmaktadır. Serbest enerji salan bir kimyasal tepkime kendiliğinden gerçekleşebilir. Gerekli aktivasyon enerjisi oldukça yüksek olduğundan, biyokimyasal tepkimeler katalizör katılmadığında son derece yavaş gelişirler. Katalizörler, enzimler de dahil olmak üzere, ne tepkimenin denge sabitini, ne de serbest enerjideki net değişimi etkilerler. Kendi başlarına, bir tepkimenin yukarı doğru olmasını sağlayamazlar, ama aşağı doğru ilerleyen belirli tepkimelerin çok daha hızlı gerçekleşmesini sağlarlar.
Enzimler aktif merkez inorganik katalizörlerin aksine yüksek özgüllüğe sahiptirler. Belirli bir enzim substrat adı verilen sadece tek ya da bir çift reaktant ile etkileşir. Örneğin trombin enzimi belirli proteinler ve belirli aktif merkezler üzerinde görev yapar. Arjinin ve glisin arasındaki bağı “tanır” ve bunu hidrolize eder (Kanı n pıhtılaşmasında önemli bir basamak). Diğer tüm katalizörler gibi, tepkime için gerekli olan aktivasyon enerjisini düşürür ve böylece birçok substrat molekülünün kinetik enerjisinin tepkimenin meydana gelebileceği düzeye ulaşmasını sağlar. Sonuç olarak enzimler katalize ettikleri tepkimeyi çok fazla hızlandırırlar, tek bir enzim molekülü, her saniyede binlerce hatta yüzbinlerce reaktant molekülün, ürün oluşturacak şekilde birleşmesini sağlar.
Verimlilik ve özgüllükleri sayesinde enzimler hem özgül substratların belirli metabolik yollara katılımını sağlarlar hem de diğer metabolik yollara girmelerini önlerler, böylece yaşam kimyasının büyük bir doğrulukla yönetilmesini sağlarlar. Biyokimyacılar uzun zamandır bu özgünlüğün anahtarının yüzey aktivitesi olduğunu bilmektedir.
Enzimler globüler proteinlerdir ve karışık üç boyutlu dış görünüşleri ve birbirinden farklı yüzey geometrileri ile oldukça karmaşık moleküllerdir. Belirli bir enzim; ancak ona moleküler konformasyonu uyan -yüklü grupların konformasyonu ve yeri- substratlarla tepkimeye girebilir. Yani, bir enzimin özgüllüğü, onun üç boyutlu konformasyonuna bağlıdır.
Proteinlerin denatüre olduklarında -üç boyutlu yapıları bozulduğunda- biyolojik aktivitelerini kaybettiklerinin ve enzimatik kaybolduğunun gözlenmesi enzimlerin aktivitilerenin üç boyutlu yapılarına bağlı olduğu sonucunu ortaya çıkarmıştır. Ayrıca, birçok enzimin pH değişimlerine son derece duyarlı olması ve sadece çok kısıtlı pH aralıklarında aktif olmaları da bu sonucu desteklemiştir. Görünüşe göre, pH’daki değişiklikler proteinlerin konformasyonlarını kararlı kılan zayıf bağların kırılmasına aynı zamanda proteinin şeklinde değişikliklere neden olacak yeni bağların kurulmasına neden olmaktadır.
![Enzimler]() Enzim Substrat
Enzim Substrat
Enzim ve substratın birbirine uyumu, anahtar-kilit ya da bir bulmacanın parçaları şeklinde hayal edilebilir. Ve eğer birleşeceklerse kabaca komplementer olmaları gerektiği bir gerçektir. Platin ile oksijen ve hidrojenin bağlanması gibi, substrat molekülünün reaktif kısmı ile enzimin aktif merkez olarak bilinen bir bölgesinin geçici bir bağ kurabilecek kadar uygun olması gerekir. Bu şekilde, enzim-substat kompleksi denen geçiş formunu oluştururlar. Fakat enzimler ve onların substratları ES kompleksini oluşturabilmeleri için her zaman birbirlerine konformasyonel açıdan uygun olmak zorunda değildir, geniş ölçüde kabul gören induced-fit hipotezine göre birçok ezim bağlanma esnasında tam uyumu kuvvetlendirecek konformasyonal değişikliğe uğrar ve ES’i daha reaktif hale getirir.
Uzaysal uygunluk, enzim substrat ilişkisi için ön koşullardan sadece bir tanesidir. Bir diğeri ise, E ve S’nin kimyasal olarak da uygun olması ve birbirleriyle çok sayıda ve önemli zayıf bağlar kurabilmeleridir. Enzim ve substrat molekülleri kimi zaman kovalent bağlarla bir arada tutuluyorsa da daha çok protein konformasyonunu kararlı kılan zayıf bağlara iyonik, hidrojen, van der Walls rastlanır. Bu bağlar, normal sıcaklıklarda, ısısal hareket nedeniyle oluşan rastgele çarpışmalar sonucu, hızlı bir şekilde oluşup, kırılabilirler.
Belirli bir enzim molekülüne hangi tip substratın bağlanabileceği, enzimin aktif merkezini oluşturan amino asitlere -özellikle bu amino asitler üzerindeki R gruplarına ve bu grupların birbirlerine göre uzaysal konumlarına bağlıdır. Bir enzimin aktif merkezinin substrat molekülünün reaktif kısmının uyabileceği kavisli bir oluk şeklinde olduğunu varsayalım. Ve varsayalım ki, bu olukta yer alan amino asitlerin çoğunun R grupları elektrik yüklü olsun. Substrat molekülünün reaktif kısmının da uygun elektrik yüklü ya da polar olması gerektiği açıktır; elektriksel olarak nötral ve polar olmayan bir subtrat molekülünün ya da aktif merkezle aynı elektrik yüküne sahip bir subtrat molekülünün, şans eseri olarak uyum sağlasa bile, enzimin aktif merkezi ile tepkimeye girmesi mümkün değildir. Tersine, aktif merkezi büyük hidrofobik R grupları içeren bir enzimle sadece hidrofobik bir substrat etkileşebilir, elektriksel olarak yüklü ya da polar moleküller, bu şekildeki bir merkeze uygun değildir.
![Enzimler]() Koenzim, Kofaktör
Koenzim, Kofaktör
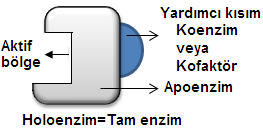
Prostetik grupları olmayan bazı enzimler katalizledikleri tepkime sırasında zayıf ve geçici olarak bağlandıkları kofaktörler içerirler. Kofaktör, metal iyonları olabilecekleri gibi, koenzim olarak adlandırılan protein olmayan organik moleküller olabilirler. Koenzim molekülleri protein moleküllerinden daha küçük ve daha az komplikedir. Enzimler gibi onlar da, girdikleri tepkimelerde tüketilmez ve değişikliğe uğramazlar ve bundan dolayı, tekrar tekrar kullanılabilirler.
Kofaktörler çok küçük miktarlarda yeterli olmalarına karşın eğer kaynak normalin altına düşerse, organizmanın sağlığı, hatta yaşamı tehlikeye düşer. Bu yüzden önemli koenzimlerin parçaları olan vitaminler beslenmemizde çok gereklidir.
Enzim Aktivitesinin Kontrolü
Enzimler, yaşayan organizmalardaki sayısız kimyasal tepkimeleri kontrol ettiklerinden, bunların kendi aktivitelerini kontrol eden çok çeşitli mekanizmalarının olması şaşırtıcı değildir. Bu mekanizmalar sadece, pH, sıcaklık ve enzim-substrat kosantrasyonu gibi fiziksel parametrelere değil regülasyonlarına yardımcı oldukları enzimlerin aktif merkezlerini maskeleyen, bloke eden ya da değiştiren kimyasal ajanlara da bağlıdır.
Kompetetif inhibisyon olarak adlandırılan enzim kontrolünün yaygın bir formunda, normal substrat molekülüne son derece benzeyen ve enzimin aktif merkezine tersinir şekilde bağlanan inhibitör maddeler söz konusudur. Bu maddelerin, substrattan farkı, tepkime sırasında kimyasal değişime uğramamasıdır. Örneğin substrat molekülünde normal olarak kırılan bir bağ, inhibitör maddede kırılmayacak kadar çok kuvvetli ya da yakınındaki bağlarla çok iyi çevrelenmiş olabilir. İnhibitor aktif merkeze bağlanarak onu maskeler ve normal substrat molekülün aktif merkeze giriş yolu bulmasını engeller. Bu şekilde Enzim+İnhibitör = “Eİ” tepkimesi aynı enzimle çalışan ve az miktarda yer alan Enzim+Substrat= ES – E+P tepkimesiyle yarışa girer. İki tepkimeden hangisinin üstün geleceği, bunların bağıl enerjilerine ve daha çok I ve S’nin bağıl konsantrasyonlarına bağlıdır. Eğer fazla inhibitör ve az miktarda substrat molekülü varsa yüksek orandaki enzimin büyük bir kısmı EI olarak bağlanır ve bu yüzden tükenir. Bunun aksine eğer fazla miktarda S ve sadece az miktarda I varsa, bu durumda enzim moleküllerinin çoğu ürünü oluşturmak üzere substrat molekülleri ile olan tepkimeyi katalizlemek üzere serbest olacaktır.
 Karbonmonoksit zehirlenmesi kompetetif inhibisyonun bir örneğidir. Karbonmonoksit, omurgallıların kanında, vücut hücrelerine oksijen taşımakla görevli enzim benzeri bir molekül olan hemoglobinin aktif merkezine bağlanmak için oksijenle yarışır. Karbonmonoksit, aktif merkeze öyle kuvvetle bağlanır ki, oksijeni tamamen saf dışı eder. Dahası, bu inhibisyon önemli derecede tersinmezdir; bir kere bağlandı mı, karbonmonoksit yerini korur.
Karbonmonoksit zehirlenmesi kompetetif inhibisyonun bir örneğidir. Karbonmonoksit, omurgallıların kanında, vücut hücrelerine oksijen taşımakla görevli enzim benzeri bir molekül olan hemoglobinin aktif merkezine bağlanmak için oksijenle yarışır. Karbonmonoksit, aktif merkeze öyle kuvvetle bağlanır ki, oksijeni tamamen saf dışı eder. Dahası, bu inhibisyon önemli derecede tersinmezdir; bir kere bağlandı mı, karbonmonoksit yerini korur.
Oksijen kaybı sonucunda yaşayan dokular, özellikle beyin dokusu, karbon monoksit miktarı bağıl olarak düşük olsa da zarar görebilir ya da ölüme sürüklenebilir. Gerçi, birçok kompetetif inhibitör hedeflerine sadece kısa bir süre için bağlanır, bu tersinir inhibisyon, inhibitör ve substratı n her zaman bir yarış içinde olduğu anlamına gelir, ikisinden birinin konsantrasyonundaki bir değişiklik, anında enzim aktivitesindeki değişme olarak yansır.
Non-kompetetif inhibisyon olarak adlandırılan tersinir inhibisyonun diğer bir tipinde, aynı enzim molekülü üzerinde iki tip bağlanma bölgesi: substratın bağlanacağı normal aktif merkez ve inhibitörlerin bağlanabileceği diğer merkezler bulunur. Non-kompetetif inhibisyonun en yaygın olanı allosterik inhibisyondur. Bir alostrik enzim, genellikle tersiyer yapıdaki farklılıkları yansıtan, iki farklı uzaysal konformasyonda görülebilen bir enzimdir. Çoğunlukla molekülün bir konformasyonunda enzim aktifken, diğer konformasyonunda substrat bağlayan merkez engellendiğinden enzim inaktiftir (ya da daha az aktiftir). Allosterik inhibisyonda inhibitör maddelerin bağlanması- genellikle negatif modülatör ya da negatif effektör enzimin inaktif konformasyonunu kararlı kılar. Genellikle ürünün kendisi ya da aynı biyokimyasal yolda, daha sonraki bir tepkimenin ürünü modülatör rolünü üstlenir. Daha fazla gereksinme olmayan yüksek konsantrasyonlara ulaştığında kendi sentezinden sorumlu olan işlemi durdurur. Bu şekil de ürünün kendini kısıtlamasına “feedback inhibisyon” denir. Diğer allosterik enzim tipleri ise enzim aktivitesini arttıracak, konformasyonel değişikliklere neden olan pozitif modülatörler için bağlanma merkezlerine sahiptir.
Bazı allosterik enzimlerde ise farklı tip bağlanma merkezleri yerine, aynı tip merkezden iki ya da daha fazla bulunur ve böylece substratı iki ya da daha fazla bölgede aynı anda bağlar. Bir aktif merkeze bir substratın bağlanışı diğer merkezleri daha reaktif hale getirecek konformasyonel değişimlere neden olur. Kooperativite olarak adlandırılan bu olay hemoglobinde örneklenmiştir. Tek bir hemoglobin molekülü, dört oksijen molekülü taşıyabilir. İlk oksijen molekülünün bağlanması, hemoglobin molekülünün kuvarterner yapısında, diğer üç bağlanma bölgesine oksijen için daha yüksek affinite kazandıracak değişikliklere neden olur. Böylece kooperativitede bağlanan ilk substrat molekülü, modülatör olarak işlev görür. Allosterik proteini mümkün olan en uygun konformasyonda tutar (hemoglobin söz konusu olduğunda en reaktif konformasyonda).
 Kompetatif inhibitörlerin, nonkompetatif inhibtörlerin ve allosterik modülatörlerin, enzimin aktif merkezleri üzerindeki farklı etkileri sayesinde, kimyacılar, bunları enzimlerin doğasını araştırmada fazlasıyla değerli oldukları kanısına varmışlardır. Mesela aktif merkez konusunda daha açık bir fikre sahip olmak için-fiziksel şekli ve reaktif R grupları – çok az farklılıklara sahip bir seri kompetetif inhibitörler sentezleyip bunların her birinin aktif merkeze bağlanmadaki etkilerini çalışabilirler. Bir enzim molekülünün farklı kısımlarının rollerini araştırmak için, tersinmez inhibitörlerden -kataliz tepkime için gerekli işlevsel gruplar ile kalıcı kovalent bağlar yaparak enzim zehirleri gibi görev alan kimyasallardan- faydalanırlar. Son zamanlardaki moleküler biyoloji teknikleri, enzimdeki her bir peptitin seçici yer değiştirme ve delesyonuna imkan vermeye başlamıştır. Sonuç olarak, bir proteinin herhangi bir amino asitinin görevi deneysel olarak keşfedilebilir. Günümüzde biyokimyaclar, bu tekniğin getirdiği bilgilerin sonuçlarından biri olarak, yapay bir enzim planlayıp, sentezleyebilir. Bu “düzenlenen enzimler” doğada bilinmeyen aktivite ve özellikte hazırlanabilir. Bu tip enzimler hastalıklarla mücadelede ve hatta çevresel kirlilik problemlerinin çözümünde sınırsız potansiyele sahip olabilir.
Kompetatif inhibitörlerin, nonkompetatif inhibtörlerin ve allosterik modülatörlerin, enzimin aktif merkezleri üzerindeki farklı etkileri sayesinde, kimyacılar, bunları enzimlerin doğasını araştırmada fazlasıyla değerli oldukları kanısına varmışlardır. Mesela aktif merkez konusunda daha açık bir fikre sahip olmak için-fiziksel şekli ve reaktif R grupları – çok az farklılıklara sahip bir seri kompetetif inhibitörler sentezleyip bunların her birinin aktif merkeze bağlanmadaki etkilerini çalışabilirler. Bir enzim molekülünün farklı kısımlarının rollerini araştırmak için, tersinmez inhibitörlerden -kataliz tepkime için gerekli işlevsel gruplar ile kalıcı kovalent bağlar yaparak enzim zehirleri gibi görev alan kimyasallardan- faydalanırlar. Son zamanlardaki moleküler biyoloji teknikleri, enzimdeki her bir peptitin seçici yer değiştirme ve delesyonuna imkan vermeye başlamıştır. Sonuç olarak, bir proteinin herhangi bir amino asitinin görevi deneysel olarak keşfedilebilir. Günümüzde biyokimyaclar, bu tekniğin getirdiği bilgilerin sonuçlarından biri olarak, yapay bir enzim planlayıp, sentezleyebilir. Bu “düzenlenen enzimler” doğada bilinmeyen aktivite ve özellikte hazırlanabilir. Bu tip enzimler hastalıklarla mücadelede ve hatta çevresel kirlilik problemlerinin çözümünde sınırsız potansiyele sahip olabilir.
Kaynakça:
https://www.khanacademy.org
Yazar: Taner Tunç


