Otopsi yapılan insan doku bölümlerinde mikroglia sınıflandırmasındaki başarı, öncelikle bu amaç için kullanılan antikorlara ve aynı zamanda çalışılan beyin dokusunun nasıl korunduğuna bağlıdır. İmmünohistokimya için mikroglial belirteçlerle ilgili yayınlanmış birçok çalışma, geniş ölçüde sabitlenmiş doku kesitlerinde güçlü immünoreaktivite üreten antikorlarla sınırlandırılmıştır. Bu, özellikle insan mikroglial çalışmaları için en yaygın olarak kullanılan HLA-DR için geçerlidir, çünkü mevcut antikorlar çok çeşitli korunmuş beyin dokusu üzerinde canlı sonuçlar verebilir.
Çalışma referanslarında HLA-DR için birincidir ve 30 yıllık çalışmaları kapsayan en son referanslardır AD mikroglia’da HLA-DR’nin işlevi hala belirsizdir. Bu protein, işlenmiş antijenleri AD mikro ortamında bulunmayan T lenfositlerine sunma işlevi görür. AD mikroglia’da HLA-DR’nin yukarı regülasyonuna yol açan sinyalleşme tanımlanmamıştır. Son yıllarda, sitoskeletal reorganizasyon ve hücre hareketliliğinde rol oynayan aktin bağlayıcı bir proteini tanıyan IBA-1 belirteci de, güçlü boyama antikorlarının mevcudiyeti nedeniyle mikroglia’yı tanımlamak için yaygın bir şekilde kullanılmıştır. IBA-1 antikorları, aktive mikrogliada sınırlı yukarı regülasyona sahip tüm mikrogliaları tanıyor gibi görünmektedir, ancak bu yorum aynı zamanda mikroglial morfoloji ile ilgili gözlemlere de bağlıdır.
Doku kesitlerinde güçlü sonuçlar üreten antikorların kullanımı, diğer birçok antijenik belirteç mevcut olduğu için, hastalıktaki mikroglial işlevi anlamamızı engellemiş olabilir, ancak bunları dokuda ortaya çıkarmak için uygun antikorlar mevcut değildir. İşlevin en yararlı markörleri, antijenikliği fiksasyon koşullarından ve ayrıca glikosilasyon derecesinden önemli ölçüde etkilenen hücre yüzeyi glikosile proteinlerdir. Birçok araştırmacı için en yaygın olarak bulunan dokular, uzun süreler boyunca formalinle sabitlenmiş ve ardından parafine (FFPE) gömülmüş doku bloklarıdır; bu süreç, ksilen ile muameleleri içerir. Bu koruma yöntemleri, antikorların birçok antijeni, özellikle de hücre yüzeyi glikoproteinlerini tanıma yeteneğini güçlü bir şekilde etkiler. 
FFPE dokusunda antijen tanımada etkili olan antikorların sayısı, mevcut antikorların küçük bir yüzdesidir. Ek olarak, FFPE dokusunun kullanımı, çoğu antikorun çalışması için genellikle antijen geri kazanım tekniklerinin uygulanmasını gerektirir; bu yöntemlerin bir dizi vardır ancak bunların başarılı bir şekilde uygulanması operatör becerisine bağlıdır ve tekrarlanabilir olmayabilir. Belirtildiği gibi, insan beyni örneklerinde mikrogliayı sınıflandırmak için M1 ve M2 benzeri şemaların uygulanabilirliği eleştirilmiştir, çünkü sınıflandırma antijenlerinin çoğu doku mikroglialarında kanıtlanmamıştır FFPE dokusunda antijen tanımada etkili olan antikorların sayısı, mevcut antikorların küçük bir yüzdesidir.
AD’de Mikroglial Fonksiyonel Proteinlerle İlgili Önceki Çalışmalar
AD’li beyinlerde mikroglia tarafından patoloji ile ilişkili alanlarda artan HLA-DR ekspresyonunun ilk çalışmalarından bu yana AD’li beyne bir dizi makrofaj belirtecinin ekspresyonu uygulanmıştır. Dokular. Bunlar arasında beta II integrinleri (CD11a, b ve c ve CD18 – tamamlayıcı ve fagositik reseptörler), immünoglobulin Fc reseptörleri (CD16, CD32, CD64), lipopolisakkarit reseptörü CD14, makrofaj koloni uyarıcı faktör reseptörü-1 (CSF-1R; CD115), tip B çöpçü reseptörü CD36, ferritin, sinyal düzenleyici protein beta-1 ve progranulin bulunur. CD43 ve TMEM106B belirteçlerinin, kontrollere kıyasla AD mikrogliada aşağı regüle edildiği gösterilmiştir. Bu, alan sınırlamaları nedeniyle eksik bir listeyi temsil eder, ancak bu belirteçlerin çoğu sitotoksisiteden ziyade fagositik işlevle ilgilidir. 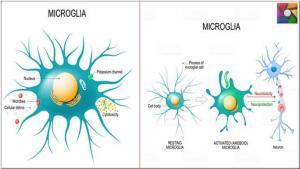
Ferritin, her yerde bulunan bir demir taşıma proteini olduğu için mikroglial aktivasyonla ilişkili benzersiz özelliklere sahiptir, ancak dokuda seçici olarak aktif mikroglia popülasyonunu belirlediği görülmektedir. Potansiyel sitotoksisiteyi doğrudan göstermek için, mikrogliada artmış sitokin seviyelerinin gösterilmesi gereklidir. Son 30 yılda, doku kesitlerinde sitokinlerin profilini çıkarmak için immünohistokimyayı kullanan çok az çalışma yapılmıştır. Griffin ve meslektaşları tarafından yapılan bir dizi çalışma, IL-1; ifade eden mikroglia’nın farklı tipte plak ve düğümlerle ilişkili olduğunu gösterdi.
Yaygın nöritik ve nöritik olmayan plaklar en fazla IL-1 a pozitif mikrogliaya sahipken, yoğun çekirdek nöritik ve nöritik olmayan plaklar önemli ölçüde az sayıda IL-1 a pozitif mikrogliaya sahipti. Bu sonuçlar, bu mikroglia popülasyonunun plak oluşumunun erken aşamalarında yer aldığını göstermektedir. Bu markörün kullanılması, IL-1pozitif mikroglianın parahipokampal girusta nörofibriler yumak oluşumunda rol oynadığını göstermiştir. Başka bir çalışmada, IL-1 ve TNF’nın insan AD dokusunda mikrogliada lokalize olabileceği gösterilmiştir. Sınırlı sayıda çalışma, sitokinler gibi salgılanan proteinleri tespit etmenin teknik zorluklarını vurgulamaktadır.
Griffin ve meslektaşları, immünohistokimya için FFPE dokusunu kullandı. Sitokinleri dokuya yerleştirmek için kısa sabitlenmiş mikrotom kesim bölümlerini kullanarak birkaç kez denedik ve hiçbir zaman başarılı olamadık. Bu moleküller, membran lokalizasyonu yerine salgılandığından, FFPE’de yer alan sert fiksasyonun onları tutturmak için ve ardından antikor erişimine izin vermek için antijen geri kazanımına ihtiyaç duyulması mümkündür. Kısa sabitlenmiş beyin dokusu materyalleri ile, bu çözünür proteinler, lokalizasyon için yerinde yeterince sabitlenmeyebilir.
Mikroglial Fenotipleme İçin Antikor Seçimi
İlgili proteinlerin yerini ortaya çıkarmak için gereken uygun antikorların seçimi söz konusu olduğunda, insan beyni immünohistokimyasının tüm alanı birkaç sınırlamaya sahiptir. İlk olarak, genellikle fare veya tavşan kökenli bir monoklonal antikor olan ve dolayısıyla hedef proteinin küçük bir bölümünü temsil eden bir epitopa özgü olan antikor, özgünlük gösterebilmelidir, yani, hedef proteini yerinde tanımaktadır.Ve diğer proteinlerle çapraz reaksiyona girmez. İkinci olarak, antikor, dokudaki hedef proteini tanıması doğrulanabilirse, özgüllüğü ve hassasiyeti fiksasyon koşullarından etkilenebilir.
Deneyimlere göre, daha geniş bir antikor yelpazesine sahip mikroglial antijenlerin incelenmesi, paraformaldehit (formalin değil) içinde kısa bir süre (48 saat) sabitlenmiş beyin dokusu kullanılarak daha az sorunlu olmuştur ve ardından dondurucu bir mikrotom kullanılarak kriyoproteksiyona tabi tutulmuş ve kesilmiştir. Bu işlem, dokunun parafine gömülmesiyle ilgili sert işlemlerden kaçınır. Yıllar içinde, mikroglial proteinler CD87, RAGE, CD33, TREM-2, TLR-2, -3, -4 ile birlikte HLA-DR, IBA-1, CD68’i başarıyla tanımlanmıştır. (AD dokuları)
Bu dokuları kullanırken antikorlarla ilgili deneyimimiz, başarılı immünolokalizasyon şansını artırmaya yardımcı olan bazı özellikleri belirlenmiştir. Bir şirket – Ar-Ge Sistemleri – Biotechne, Minneapolis, MN – endüstri için nispeten benzersiz bir strateji kullanarak antikorlarının çoğunu üretti. Antikorlarının çoğu, ökaryotik hücrelerde ifade edilen ilgi konusu proteinlerden hazırlanmıştır. Bu proteinler, insan dokularında beklenene benzer şekilde glikosile edilecektir. Ek olarak, immünize edici proteinler genellikle doğal proteinin çoğunu kaplar ve böylece birden fazla antijenik epitop içermenin yanı sıra antijenliği etkileyen ikincil protein yapısının bir kısmını korur. Bu proteinler, immünojen olarak 10-20 amino asitlik kısa sentetik peptit sekanslarını kullanan ve daha sonra hayvan immünizasyonundan önce bir taşıyıcıya konjuge olan birçok şirketin stratejisinden daha üstün immünojenikliğe sahip antikorlar üretir.
Ar-Ge Sistemleri afinite saflaştırılmış poliklonal antikorlarla ilgili deneyimimiz genellikle hafif sabitlenmiş dokularda kullanım için elverişli olmuştur. Bu antikorlar, fiksasyondan ciddi şekilde etkilenmeyen proteinler üzerindeki epitopları tanımlama olasılığını artırabilen bir dizi epitop içerecektir. Poliklonal hazırlamak için büyük protein antijenlerinin kullanılması, diğer ilgili proteinlerle çapraz reaktivite potansiyeli olduğundan bazı dezavantajlara sahiptir. Kalite kontrol, doku reaktivitesinin giderildiğini göstermek için antikorun protein absorpsiyonunu gerçekleştirebilmesine bağlıdır,
AD beyinlerinde mikrogliayı tanımlamak için Toll benzeri reseptöre (TLR) -3 (AF1487) yönelik bir Ar-Ge Sistemleri antikoru ve CD206’ya yönelik bir Ar-Ge Sistemleri poliklonal antikoru (AF2535) kullanarak deneyimimizi göstermektedir. ), Mikroglia’yı tanımlayamayan (D ve E panelleri). TLR-3 poliklonal antikoru, insan beyni mikrogliasındaki yapıları tanımlayabilir. Bir yorum, batı lekeleri beyin materyali gibi karmaşık materyal kullanılarak gerçekleştiriliyorsa, tam uzunluktaki proteinin yanı sıra diğer protein bantlarının da varlığı beklenmelidir.
İşlevsel proteinlerin çoğu ya normal işlevleri sırasında bölünür, örneğin lider sekansların kaybı, salgılanan formlar üretmek için bölünür veya hücresel metabolizmanın bir parçası olarak parçalanır. İlginç bir şekilde, aynı immünize edici protein ile üretilen TLR-3’e yönelik bir monoklonal antikor, dokuda mikroglia boyayamamıştır, ancak bu antikor, immünize edici proteinde bulunan yalnızca tek bir epitop için spesifik olacaktır. CD206’ya karşı bir Ar-Ge sistemleri antikoru ile benzer deneyimler olmuştur. Ökaryotik bir hücre eksprese edilmiş proteine karşı üretilen. Bu protein, ekspresyonu IL-4 varlığında indüklendiğinden, M2a alternatif aktivasyonu için prototip bir markör olarak tanımlanmıştır.
Bu antikoru, insan beyninde alternatif aktivasyon mikroglialarına dair kanıt olup olmadığını belirlemek için kullanılmıştır Western blotlarda beyin numunelerindeki spesifik bantları tespit edebilen bu antikoru kullanmak, boyanılan kontrol veya AD doku bölümlerinin hiçbirinde mikrogliayı tanımlamamıştır. Bununla birlikte, beyin bölümlerinde bulunan damarların içinde veya çevresinde bulunan yuvarlak hücrelerin (perivasküler makrofajlar) güçlü CD206 boyaması dikkat çekiciydi. Bu, yayınlanmış bir bulguya benzerdir. Bu, alternatif aktive edilmiş makrofajların damarlarda yaygın olduğunu gösterirken, alternatif aktive mikroglia nöropilde bulunmadığını göstermektedir.
İnsan beyinlerinde, beyin homojenatlarını kullanarak RNA veya protein seviyesinde inflamatuar ilişkili moleküllerin ekspresyonunun belirlenmesi, doku içinde önemli sayıda kan hücresi sıkışabileceğinden dikkatle yorumlanmalıdır. Mikroglia ile ilgili gözlemler yapılırken bulguların immünohistokimya ile doğrulanması gerekir. AD beyin örneklerinde alternatif aktive markörlerin yokluğu CD200 reseptörü (CD200R) için doğrulandı. Bu, anti-enflamatuar sinyali indüklemek için ligand CD200 tarafından aktive edilen miyeloid spesifik bir reseptördür. IL-4 ve IL-13 tarafından indüklendiğini ve CD206’ya benzer bir M2a markörünün klasik tanımına uyduğunu göstermektedir.
Ar-Ge Sistemleri poliklonal antikoru (AF3414) ve özel bir peptit antikoru dahil olmak üzere birkaç antikor kullanarak, CD200R’nin protein ve mRNA ekspresyonu insan beyninde saptanabilir olsa bile, CD200R immünoreaktivitesini beyin mikroglia’da lokalize edilmemiştir. Dokuda mikroglial profillemede gözden kaçmış görünen bir belirteç, LPS ko- reseptörü olan CD14’tür. Bu reseptör, proinflamatuar aktivasyon ile bağlantılı yukarı regülasyona sahip klasik bir M1 benzeri aktivasyon markörüdür. CD14 için insan AD beyinlerinde mikroglial immünohistokimyayı tanımlayan yalnızca tek bir çalışma vardır. Kısa fiksasyon dokusunu kullanarak, bu markörün ekspresyonunu yeniden incelenmiştir. Tüm vakaların çoğu vasküler makrofajı tarafından güçlü bir şekilde eksprese edilir, ancak artmış ekspresyon, AD vakalarında IBA-1 mikroglia alt kümelerinde kolayca tespit edilebilir. CD14, TLR-2 veya TLR-4 ile etkileşim yoluyla proinflamatuar aktivasyon ile Ap’yi bağlayabildiğinden, artmış CD14 ekspresyonu, sitotoksik mikrogliayı tanımlamak için daha çok kullanılan bir işaret olabilir.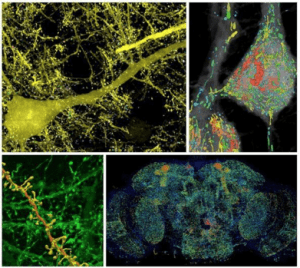
İnsan Beyninde TREM-2 Mikroglia Profilinin Çıkarılması
Bu tartışma, TREM-2 pozitif mikroglianın mikroglial fenotiplemesini dikkate almak için özellikle önemlidir. TREM-2’nin AD’deki rolüne büyük ilgi, nöroinflamasyon ve AD’ye yeni ilgiyi artırmıştır. TREM-2 genindeki (rs75932628) TREM-2 proteininde (R47H) bir mutasyona neden olan tek bir nükleotid polimorfizmi (SNP), incelenen popülasyona bağlı olarak AD gelişme riskini 2 ila 11 kat artırabilir. TREM-2 veya onun adaptör proteini DAP12’deki mutasyonlar ilk olarak Nasu-Hakola hastalığında tanımlanmıştır ve bu da diğer semptomların yanı sıra erken başlangıçlı demansa yol açar.
Mutasyon, normal işlevi apoptotik nöronların fagositozunu ısı şok proteini 70’e (hsp70) veya lipidlerin farklı biçimlerine bağlanarak teşvik etmek olan TREM-2 proteininin işlev kaybına yol açıyor gibi görünmektedir. İnsan AD beyinlerinde TREM-2’nin immünohistokimyasına ilişkin az sayıda çalışma yapılmıştır, bu temelde patolojik çalışma için sağlam antikorların eksikliğinden kaynaklanmaktadır. Plak ve karışma ile ilişkili mikroglia’nın TREM-2 için pozitif olduğunu gösteren ilk çalışmalardan birini yayınlanmıştır. Bu çalışmada, insan beyin dokusunda özgüllük ve duyarlılık için bir dizi antikoru taraması gerekir.
En iyi sonuçlar, proteinin % 75’ine ve tam hücre dışı alana karşılık gelen bir ökaryotik hücre ekspresyonu proteini kullanılarak hazırlanan TREM-2’ye (AF1828) yönelik bir R&D Systems poliklonal antikoru ile elde edilmiştir. İnsan TREM2’nin (ab175262, Abcam, Cambridge, MA) N-terminal amino asitleri 29-59’a karşılık gelen bir peptit kullanılarak hazırlanan bir antikor kullanılarak AD frontal kortekste TREM-2 ekspresyonunun yakın zamanda yapılan bir çalışması, western blotlar ile özgüllük gösterdi, ancak bu yazarlar TREM2 immünohistokimyası hakkında hiçbir veri sunmamıştır.
TREM-2 ekspresyonu, dendritik / miyeloid hücreler ile sınırlıdır ve beyin mikroglialarında yüksektir. Ticari antikorların özgüllüğü, aynı zamanda tespit hassasiyeti de bir sorun olmuştur. İki çalışma, TREM-2’nin beyindeki mikroglia tarafından eksprese edilmediği sonucuna varmıştır, ancak her iki çalışmada da antijen geri kazanımı ile FFPE doku örnekleri kullanılmıştır. Bir çalışma, AR-GE antikorunun, yayınlanmış çalışmamıza benzer şekilde TREM-2 için spesifik olduğunu, ancak mikroglial TREM-2 immünoreaktivitesini gösteremediğini göstermiştir. Önceki çalışmaya benzer şekilde, parafine gömülmemiş hafif sabitlenmiş beyin dokuları kullanılmıştır. Bu bölümlerle, mikroglia’ya spesifik TREM2 lokalizasyonunu gösterilebilmiştir. Bulgu, TREM-2’nin AD modeli transgenik farelerde plakla ilişkili mikroglia’da lokalize olması nedeniyle mantıklıdır.
Kaynakça:
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6678308/
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6678308/
Yazar: Özlem Güvenç Ağaoğlu
