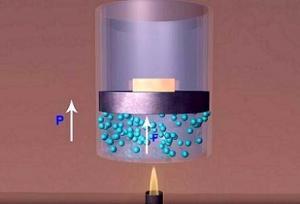
 Termodinamik, fizik biliminin, termal enerjiyi bir başka enerji biçimine (mekanik, elektrik vb.) veya işe aktarabilen sistemlerle ilgilenen dalıdır. Termodinamiğin tarihi, 1650 yılında tarihe geçen Magdeburg yarıküreleri deneyini sergileyen Otto von Guericke ile başlar. Guericke, Aristoteles’in “doğa boşluktan nefret eder” varsayımına karşı bir vakum oluşturma arayışındaydı. Guericke’nin deneyinden bir süre sonra, İrlandalı ünlü fizikçi ve kimyacı Robert Boyle (1627- 1691), Guericke’nin tasarımlarından yola çıkarak, 1656’da Robert Hooke ile birlikte bir hava pompası ürettiler. Bu pompayı denerken, basınç, sıcaklık ve hacim arasındaki ilişkiyi fark ettiler.
Termodinamik, fizik biliminin, termal enerjiyi bir başka enerji biçimine (mekanik, elektrik vb.) veya işe aktarabilen sistemlerle ilgilenen dalıdır. Termodinamiğin tarihi, 1650 yılında tarihe geçen Magdeburg yarıküreleri deneyini sergileyen Otto von Guericke ile başlar. Guericke, Aristoteles’in “doğa boşluktan nefret eder” varsayımına karşı bir vakum oluşturma arayışındaydı. Guericke’nin deneyinden bir süre sonra, İrlandalı ünlü fizikçi ve kimyacı Robert Boyle (1627- 1691), Guericke’nin tasarımlarından yola çıkarak, 1656’da Robert Hooke ile birlikte bir hava pompası ürettiler. Bu pompayı denerken, basınç, sıcaklık ve hacim arasındaki ilişkiyi fark ettiler.
Termodinamik Yasalarının Gelişimi
On sekizinci yüzyıldan başlayarak, tekstil sanayiindeki ilerlemelerin sonucunda ortaya çıkan ve insan ya da hayvanlarla karşılanamayan büyük güç gereksinimi, buhar makinelerinin bulunmasını sağladı. 1697 yılında Savery’nin, 1712 yılında Newcomen’in icat ettiği buhar makineleri, 1765’te James Watt tarafından geliştirilirken, çok sayıda araştırmacının da bu alana yönelmeleriyle, buharın özellikleri üzerine yapmış oldukları araştırmalar termodinamik bilimini de geliştirdi.
Isı enerjisinin ayrı bir enerji biçimi olarak ele alınması, bir İngiliz askeri mühendis olan Sir Benjamin Thompson (Kont Rumford olarak da bilinir), termodinamiğin birinci yasasının bir sonucu olan ve işin yapıldığı miktarla orantılı ısı üretilebileceğini fark ettiğinde, yaklaşık 1798’de başladı. Fransız fizikçi Sadi Carnot, 1824’te termodinamiğin temel ilkelerinden birini formülleştirdi. Carnot’nun ısı motoru çevrimini tanımlamak için kullandığı prensipler, Alman fizikçi Rudolf Clausius tarafından termodinamiğin ikinci yasasına dönüştürüldü.
 İlk kez Lord Kelvin’in (1824 – 1907) kullandığı termodinamik terimi, latincedeki ısı ve güç kelimelerinin birleştirilmesiyle türetildi. Termodinamik, fizik biliminin, enerjiyle ve enerjinin biçim değiştirmesiyle ilgilenen kolu ya da enerji ve entropi bilimi olarak tanımlanmakta ve yasalarından, otomobillerden uzay araçlarına, elektrik santrallerinden bilgisayarlara kadar çok çeşitli alanlarda yararlanılmaktadır. Termodinamiğin entropi kavramını, Einstein, “hiç bir zaman yerinden edilemeyecek evrensel içerikli tek fiziksel kural”, Arthur Eddington ise “evrenin en üstün yasası” olarak tanımlamışlardır.
İlk kez Lord Kelvin’in (1824 – 1907) kullandığı termodinamik terimi, latincedeki ısı ve güç kelimelerinin birleştirilmesiyle türetildi. Termodinamik, fizik biliminin, enerjiyle ve enerjinin biçim değiştirmesiyle ilgilenen kolu ya da enerji ve entropi bilimi olarak tanımlanmakta ve yasalarından, otomobillerden uzay araçlarına, elektrik santrallerinden bilgisayarlara kadar çok çeşitli alanlarda yararlanılmaktadır. Termodinamiğin entropi kavramını, Einstein, “hiç bir zaman yerinden edilemeyecek evrensel içerikli tek fiziksel kural”, Arthur Eddington ise “evrenin en üstün yasası” olarak tanımlamışlardır.
Termodinamiğin Dört Yasası
Termodinamiğin dört yasası vardır ve bunlar fizik biliminin en önemli yasaları arasındadır:
Termodinamiğin Sıfırıncı Yasası:
Eğer iki termodinamik sistemin her biri üçüncü bir sistemle ısıl dengede ise, birbirleriyle de ısıl dengededirler. Bu yasaya “sıfırıncı” denilmesi, diğer üç yasanın ardından gelmiş olmasındandır. Bu yasanın önemi tam olarak anlaşılmadan önce, diğer yasalar bir süre kullanılmış, bu temel yasanın önemi ortaya çıktıktan sonra, diğerlerini yeniden adlandırmak yerine, “sıfırıncı yasa” olarak adlandırıp ilk sıraya konulmuştur. Temel olarak, A = B ve C = B ise A = C’dir. İlk bakışta çok basit görünse de, bu yasa olmadan, sıcaklıklar tanımlanamazdı ve termometreler üretilemezdi.
 Termodinamiğin Birinci Yasası:
Termodinamiğin Birinci Yasası:
Enerji ne yaratılabilir, ne de yok edilebilir. Sadece biçim değiştirebilir. Herhangi bir süreçte, evrenin toplam enerjisi aynı kalır. Sisteme verilen net ısı, sistem tarafından yapılan net işe eşittir. Termodinamiğin birinci yasası temel olarak enerjinin korunduğunu belirtmektedir. Yasa, “Yalıtılmış bir sistemdeki toplam enerji miktarı korunur.” biçiminde de söylenebilir. Bir sistemdeki enerji, ısıya, işe ya da başka şeylere dönüştürülebilir, ancak sondaki toplam her zaman başlangıçtaki toplamla aynıdır.
Termodinamiğin İkinci Yasası:
Dengede olmayan izole bir sistemin entropisi, zamanla artar ve dengede maksimum değere yaklaşır. Bu yasa, muhtemelen yasaların en ünlüsü ve tüm bilimlerin en önemli yasaları arasındadır. Evrenin entropisi azamiye eğilim gösterir. Başka bir deyişle, evrenin entropisi ya aynı kalır ya da büyür, ama asla eksiye gitmez.
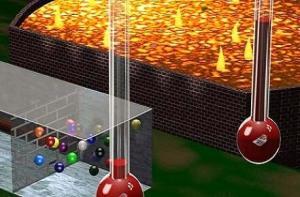
Sorun şu ki, bu yasa her zaman doğru da değildir. Bir kutudaki dört atomu örnek alırsak, dördünün de bir köşede bulunabilmeleri, oldukça düzenli bir sistem demektir ve bu yüzden düşük bir entropiye sahiptir. Ancak, zamanla dağılabilirler ve entropiyi arttırabilirler. Ama, onların köşeye rastgele geri dönmelerini engelleyen bir şey de yoktur. İnanılmaz bir olasılık, ama imkansız değil. Soruna faz alanı açısından bakıldığında da, zamanla daha büyük bir kutuya geçmeleri olasılığının, daha yüksek bir entropi anlamına geldiği görülür. Ancak, küçük olan kutuya geri dönmelerini önleyen bir engel de yoktur.
 4) Termodinamiğin Üçüncü Yasası:
4) Termodinamiğin Üçüncü Yasası:
Sıcaklık mutlak sıfır noktasına yaklaştıkça, bir sistemin entropisi sabit asgariye yaklaşır. Üçüncü yasa, entropiyi ölçmek için mutlak bir referans noktası sağlamaktadır. Bir sistemin sıcaklığı mutlak sıfıra yaklaştıkça (−273,15 °C, 0 K), entropinin değeri minimuma yaklaşır. Entropinin değeri genellikle 0 K’da 0’dır, ancak bazı durumlarda sistemde hala az miktarda entropi vardır.
Kaynakça:
– Yunus A. Cengel, Michael A. Boles, “Thermodynamics: An Engineering Approach”, McGraw Hill Education, (2017).
– Peter Atkins, “The Laws of Thermodynamics: A Very Short Introduction”, OUP, Oxford.
Yazar: Oben Güney Saraçoğlu
