 Endoplazmik retikulum (ER), hücredeki en büyük organeldir ve ana görevleri; protein sentezi ve taşınması için bir bölge olması, protein katlama, lipit ve steroid sentezi, karbonhidrat metabolizması ve kalsiyum depolamasıdır. Bu organelin çok işlevli doğası, eşsiz bir fiziksel yapıyı gerektirir. Bu nedenle ER’nin hücre çekirdeğinin çevresine yayılmış büyük bir yüzeyi ve çok sayıda kanalı vardır. ER’un çok sayıda farklı, yapısal bölmeleri vardır ve bu bölmelerden her biri belli bir fonksiyonla ilişkilidir. Fakat bu fonksiyonel bölmelerin nasıl düzenlendiği henüz bilinmiyor.
Endoplazmik retikulum (ER), hücredeki en büyük organeldir ve ana görevleri; protein sentezi ve taşınması için bir bölge olması, protein katlama, lipit ve steroid sentezi, karbonhidrat metabolizması ve kalsiyum depolamasıdır. Bu organelin çok işlevli doğası, eşsiz bir fiziksel yapıyı gerektirir. Bu nedenle ER’nin hücre çekirdeğinin çevresine yayılmış büyük bir yüzeyi ve çok sayıda kanalı vardır. ER’un çok sayıda farklı, yapısal bölmeleri vardır ve bu bölmelerden her biri belli bir fonksiyonla ilişkilidir. Fakat bu fonksiyonel bölmelerin nasıl düzenlendiği henüz bilinmiyor.
Protein Sentezi ve Katlanması
ER’un en önemli işlevlerinden biri, salgılanacak proteinler ve zar proteinlerinin sentezi için bir bölge görevi yapmasıdır (zarların nasıl sentezlediği ile ilgili daha fazla bilgi için: https://www.bilgiustam.com/hucre-zarlari-nasil-sentezlenir/). Protein sentezi için ribozomların ER’un sitoplazmaya (hücrede organeller arasındaki sıvı kısım) bakan kısmına konumlanması gerekir.
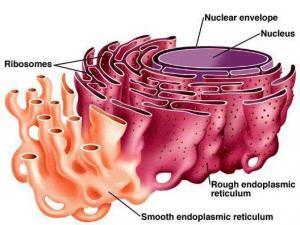 ER’a gidecek proteinler, ribozomda sentezlendikten sonra, protein dizilerindeki sinyal peptidi SRP isimli bir partikül tarafından tanımlanır. SRP ile kompleks oluşturan protein ER’deki SRP reseptörü aracılığıyla ER’a gelir. Sentezi tamamlanan proteinin ER’da sinyal dizisi kesilir. Sentezlenmiş olan protein bu aşamada düz bir amino asit zinciri halindedir ve bu proteinin işlevini gerçekleştirebilmesi için kendine özgü bir üç boyutlu yapıyı alması gerekir. Bu üç boyutlu yapıyı da, ona bir takım kimyasal gruplar ekleyen ve zincirini çeşitli şekillerde katlayan proteinler yoluyla alır. Bu üç boyutlu yapı kazanma olayı protein ER’a ulaştığında protein katlama enzimleri ve şaperonlar (proteini katlayan özel bir tür protein) tarafından gerçekleştirilir. Proteinin geçirdiği kimyasal reaksiyonlar; N-bağlı glikosilasyon, disülfit bağlarının oluşturulması ve oligomerizasyondur.
ER’a gidecek proteinler, ribozomda sentezlendikten sonra, protein dizilerindeki sinyal peptidi SRP isimli bir partikül tarafından tanımlanır. SRP ile kompleks oluşturan protein ER’deki SRP reseptörü aracılığıyla ER’a gelir. Sentezi tamamlanan proteinin ER’da sinyal dizisi kesilir. Sentezlenmiş olan protein bu aşamada düz bir amino asit zinciri halindedir ve bu proteinin işlevini gerçekleştirebilmesi için kendine özgü bir üç boyutlu yapıyı alması gerekir. Bu üç boyutlu yapıyı da, ona bir takım kimyasal gruplar ekleyen ve zincirini çeşitli şekillerde katlayan proteinler yoluyla alır. Bu üç boyutlu yapı kazanma olayı protein ER’a ulaştığında protein katlama enzimleri ve şaperonlar (proteini katlayan özel bir tür protein) tarafından gerçekleştirilir. Proteinin geçirdiği kimyasal reaksiyonlar; N-bağlı glikosilasyon, disülfit bağlarının oluşturulması ve oligomerizasyondur.
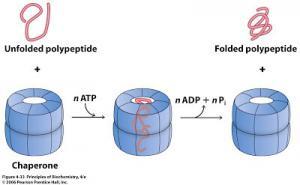 Şaperonlar ve enzimler mevcut olsa da, proteinler bazen doğru şekilde katlanamaz ve yanlış şekilde katlanmış proteinler hücrede birikir. Bu proteinler ER’de kalabilir ya da proteasomlar (protein parçalayan enzimler) tarafından ER ilişkli parçalama yolağına girer. Yanlış katlanan proteinlerin tanınmasının ardından bu proteinler ERAD yolağı tarafından parçalanır. İlginç şekilde, ER stres cevabını aktifleştiren birkaç yol vardır. Alzheimer Hastalığı gibi birkaç nörodejeneratif proteinin yanlış katlandığı hastalık, ER stres cevabı yolağını aktifleştirir. Buna ek olarak, ER stres cevabının aktivasyonu diyabette, inflamatuar bağırsak hastalığı ve çeşitli kanserlerde de görülür. ER stres cevabının hastalık patolojisinde nasıl rol oynadığı aktif bir araştırma alanıdır ve tedavi için potansiyel bir hedef olarak ER stres cevabının bileşenleri araştırılmaktadır.
Şaperonlar ve enzimler mevcut olsa da, proteinler bazen doğru şekilde katlanamaz ve yanlış şekilde katlanmış proteinler hücrede birikir. Bu proteinler ER’de kalabilir ya da proteasomlar (protein parçalayan enzimler) tarafından ER ilişkli parçalama yolağına girer. Yanlış katlanan proteinlerin tanınmasının ardından bu proteinler ERAD yolağı tarafından parçalanır. İlginç şekilde, ER stres cevabını aktifleştiren birkaç yol vardır. Alzheimer Hastalığı gibi birkaç nörodejeneratif proteinin yanlış katlandığı hastalık, ER stres cevabı yolağını aktifleştirir. Buna ek olarak, ER stres cevabının aktivasyonu diyabette, inflamatuar bağırsak hastalığı ve çeşitli kanserlerde de görülür. ER stres cevabının hastalık patolojisinde nasıl rol oynadığı aktif bir araştırma alanıdır ve tedavi için potansiyel bir hedef olarak ER stres cevabının bileşenleri araştırılmaktadır.
Lipit Biyogenezi
ER, protein sentezi için önemli bir bölge olmasının yanı sıra, sentezlenecek zarlar için de lipit biyogenezinin gerçekleştiği bölgedir. Lipitler ve proteinler ER’de modifiye edilir. Lipitler bu aşamadan sonra vesiküller yoluyla Golgi aygıtına gelir. Golgi aygıtında gerçekleşen final modifikasyondan sonra vesiküller aracılığıyla Golgi aygıtından da ayrılır.
Kalsiyum Metabolizması
 ER hücre içerisindeki kalsiyum iyonlarının depolandığı bölgedir. Hücredeki kalsiyum seviyesi düştüğünde, ER yapısında bulunan kalsiyum kanalları aracılığıyla sitoplazmaya kalsiyum salar. GPCR reseptörü tarafından fosfolipaz C uyarıldığında kalsiyum salınımı gerçekleşir. Fosfolipaz C, PIP2 molekülünü IP3’e dönüştürür. IP3’te kalsiyum iyonlarına bağlanarak salınımı kontrol eder.
ER hücre içerisindeki kalsiyum iyonlarının depolandığı bölgedir. Hücredeki kalsiyum seviyesi düştüğünde, ER yapısında bulunan kalsiyum kanalları aracılığıyla sitoplazmaya kalsiyum salar. GPCR reseptörü tarafından fosfolipaz C uyarıldığında kalsiyum salınımı gerçekleşir. Fosfolipaz C, PIP2 molekülünü IP3’e dönüştürür. IP3’te kalsiyum iyonlarına bağlanarak salınımı kontrol eder.
Hücrede gözlenen kalsiyum iyonu salınımı; döllenme sırasında spermin yumurtaya girişinden sonra, kas kasılma ve nöronlarda nörotransmitter salınımının ardından gözlenir.
ER’nin Şeklinin ve Fonksiyonunun Düzenlenmesi
ER’nin yapısı ve bölgelerinin dağılımı; çeşitli integral zar proteinleriyle, diğer organellerle ve hücre iskeletiyle etkileşimleri tarafından düzenlenir. Bu etkileşimler dinamiktir ve hücre döngüsü, hücre farklılaşması, intrasellülar sinyaller ve protein etkileşimleri gibi hücrenin durumundaki değişiklikleri yansıtır. ER nükleer zarftan ve düz tübülleri ve dalgalı kısımları içeren periferal ER’den oluşur.
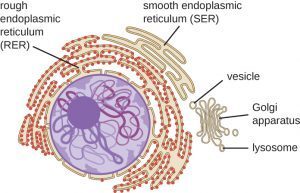 Nükleer zarf iki lipit tabakasından oluşur. Bu tabakada, protenler ve RNA’lar dahil çok sayıda molekülün geçmesine olanak taşıyan yüzlerce por (delik) vardır. Periferal ER;’nin dış kısımı iki tabaka lipit zar içerir ve dalgalı yapıdadır. Dalgalı yapıların üzerinde fazla miktarda ribozom vardır.
Nükleer zarf iki lipit tabakasından oluşur. Bu tabakada, protenler ve RNA’lar dahil çok sayıda molekülün geçmesine olanak taşıyan yüzlerce por (delik) vardır. Periferal ER;’nin dış kısımı iki tabaka lipit zar içerir ve dalgalı yapıdadır. Dalgalı yapıların üzerinde fazla miktarda ribozom vardır.
ER’nin yapısı hücre tiplerine göre de farklılık gösterir. Örneğin; pankreas gibi hormon salgılayan hücrelerde ER düz yapıdadır. Karaciğere ve kas hücreleri gibi lipit sentezi ve kalsiyum sinyali ile ilgili olan hücrelerde ise tübüler yapıdadır.
ER Stresi Varlığında ER yapısındaki Değişiklikler
Şaperonların ve enzimlerin varlığına rağmen ER içerisinde hatalı şekilde katlanmış proteinlerin varlığı ER stresi olarak tanımlanan duruma yol açar. Hücre bu şekilde bir strese girdiğinde, hücredeki dengenin sağlanabilmesi için; protein sentezinin durdurulması, yanlış şekilde katlanmış proteinlerin parçalanması ve şaperonların ve katlama enzimlerinin miktarının artması gerekir. Eğer hücre bu konuda dengeyi sağlayamazsa hücre ölümü gerçekleşir. Çünkü, yanlış katlanmış proteinler işlevlerini gerçekleştirmeden hücre içerisinde birikerek yer kapladığı için, bu durum hücredeki olayların dengesi açısından ciddi bir sorundur.
Protein ER’ye geldiğinde glikosilasyon reaksiyonu (proteine glikoz grupları eklenir) gerçekleşir. OST enzimi de proteinin yapısındaki asparajin amino asitlerini modifiye eder. Yanlış katlanma; fazla miktarda olan protein konsantrasyonundan ve şaperon gibi davranan proteinlerden kaynaklanır. Eğer protein doğru bir şekilde modifiye edilmezse, glikoz kalıntılarının yokluğu ER tarafından tespit edilir ve UGGT adlı enzim proteine glikoz grupları ekler. Eğer normal katlanma süreci gerçekleşmezse, proteindeki hidrofobik gruplar (sudan uzaklaşan bölgeler) Grp782e bağlanır, bu proteinin birikimi devam ederse, katlanmamış protein cevabı (UPR) bir savunma mekanizması olarak ortaya çıkar. UPR’nin ilk eylemi, ER’nin genişlemesini sağlamak ve katlanmayı sağlayan proteinlerin sayısını arttırmaktır.
 UPR, stres tarafından aktifleşen üç paralel yolak içerir. Bunlar IRE1 enzimimi, PERK enzimi ve ATF6 enzimidir. Bu yolakların aktivasyonu, UPR genlerini aktive eden b-ZIP transkripsiyon faktörlerinin üretimine yol açar. İlk olarak IRE1 enzimi, UPR genlerini aktifleştiren bir transkripsiyon faktörü olan XBP1 mRNA’sını kırpar. Stresin varlığında, XBP1 ve diğer yolaklar şaperonları kodlayan genlerin aktifleşmesini ve şaperon üretimini sağlar. Bu aşamadan sonra stres devam ederse hücre ölümü gerçekleşir.
UPR, stres tarafından aktifleşen üç paralel yolak içerir. Bunlar IRE1 enzimimi, PERK enzimi ve ATF6 enzimidir. Bu yolakların aktivasyonu, UPR genlerini aktive eden b-ZIP transkripsiyon faktörlerinin üretimine yol açar. İlk olarak IRE1 enzimi, UPR genlerini aktifleştiren bir transkripsiyon faktörü olan XBP1 mRNA’sını kırpar. Stresin varlığında, XBP1 ve diğer yolaklar şaperonları kodlayan genlerin aktifleşmesini ve şaperon üretimini sağlar. Bu aşamadan sonra stres devam ederse hücre ölümü gerçekleşir.
ER’daki stres cevabının mekanizmasının anlaşılması ve hastalık tedavisi için bu mekanizmanın manipüle edilmesi, Alzheimer ve Parkinson gibi yanlış katlanan proteinlerin hücre içerisinde biriktiği sinirsel hastalıkları için bir tedavi geliştirilmesini sağlayabilir.
Kaynakça:
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4700099/
Yazar: Ayça Olcay
