Kanada’daki bilim insanları, CRISPR-Cas9 genom editleme teknolojisini (genomda değişiklik yapabilmek için kullanılan bir yöntem, ayrıntılı bilgi için: https://www.bilgiustam.com/gen-duzenlemesi-yontemleri-ile-genetik-hastaliklar-tedavi-edilebilir-mi/), glioblastoma (yetişkinlerde ortaya çıkan ve en yaygın olarak görülüen beyin tümörü tipi) tedavisinde potansiyel yeni hedefleri belirlemek için kullandı. Bu yaklaşımda genom editleme; 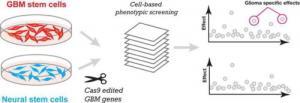 hastalardan alınan, tümör üretebilen glioblastoma kök hücrelerinin genlerinde değişiklik yapılması ve tümör gelişimi için gerekli olan genlerin tanımlanması için kullanıldı. Çok sayıda potansiyel glioblastoma belirtecinin tanımlanmasına ek olarak çalışmalar, temozolomide (TMZ) kemoterapisine karşı glioblastoma direnci mekanizmasına yeni bir bakış açısı ve potansiyel terapi stratejileri sağlar. Bu çalışma CRISPR taramasının, hastalardan izole edilmiş çok sayıda hücrede kullanıldığı ilk çalışmadır.
hastalardan alınan, tümör üretebilen glioblastoma kök hücrelerinin genlerinde değişiklik yapılması ve tümör gelişimi için gerekli olan genlerin tanımlanması için kullanıldı. Çok sayıda potansiyel glioblastoma belirtecinin tanımlanmasına ek olarak çalışmalar, temozolomide (TMZ) kemoterapisine karşı glioblastoma direnci mekanizmasına yeni bir bakış açısı ve potansiyel terapi stratejileri sağlar. Bu çalışma CRISPR taramasının, hastalardan izole edilmiş çok sayıda hücrede kullanıldığı ilk çalışmadır.
Glioblastoma hem hastalar arasında hem de tek bir hastanın vücudunda çok fazla heterojenite (farklılık) gösterir. Bu çeşitlilik, terapiye değişken yanıt vermesiyle de birleşir. Bu tümör tipi için en son kullanılan kemoterapi formu olan temozolomide’in etkisi bile sınırlıydı. Glioblastoma hücreleri tedaviye dirençli olduğu için, tümörlerin tedavi edilmesi zordur. Hastaların hayatta kalma oranlarının arttırılabilmesi için, bu hücreleri yok etmenin yeni bir yolunun bulunması gerekiyor. TMZ’nin kanser hücrelerinin yeni mutasyonlar geliştirmesine neden olduğu ve böylece kanserin ilerlemesine sebep olduğu yönünde endişeler de mevcuttur.
Kanser gelişiminin moleküler belirteçlerinin ve bu heterojenik kanser türüne karşı ilaç cevabının daha iyi anlaşılmasına ihtiyaç vardır. Böylece yeni potansiyel tedaviler ve TMZ ile birlikte yeni tedavi stratejileri geliştirmek mümkün olabilir. Bilim insanları; tümörün içerisindeki küçük bir kök hücre grubunun glioblastomanın gelişmesine öncü olabileceğine inanıyorlar. Hastalardan alınan glioblastoma kök hücrelerinin (GSC) laboratuvar ortamında kültüre edilmesi, glioblastomanın kökeninin ve ilerleyişinin anlaşılmasını sağlar. Ayrıca bu hücre kültürleri, alındığı hastaya özgü genetik özellikleri taşır. Bu hücreler üzerinde uygulanan CRISPR gen editleme yöntemi ile de hücre çoğalması için anahtar olan genler tanımlanabilir.
Toronto Üniversitesi’ndeki araştırmacılar, hastalar arasındaki glioblastoma heterojenitesi nedeniyle, 10 farklı hastadan alınan glioblastoma kök hücre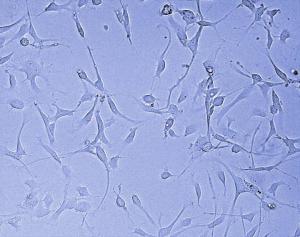 kültüründe, eş zamanlı CRISPR taraması gerçekleştirdi. Çalışmanın amacı, hücre çoğalması ve hayatta kalımının moleküler temellerini tanımlamaktı. Bu yaklaşımda, her bir hasta örneğinde tek seferde 20,000 genden her biri sistematik olarak susturuldu (işlevsiz hale getirildi). Böylece yapılan deneyde, bir genin susturulmasıyla, hücrelerde oluşan değişikler incelenerek, susturulan genin işlevinin ne olduğu anlaşılabilir. İki adet normal insan fetal nöral kök hücre kültüründeki paralel taramayla, glioblastoma kök hücre taramasının verileri karşılaştırıldı. Ayrı kemogenomik taramalar, TMZ’ye karşı tümör direnciyle ilişkili genleri ve potansiyel terapi stratejilerini tanımlamak için gerçekleştirildi.
kültüründe, eş zamanlı CRISPR taraması gerçekleştirdi. Çalışmanın amacı, hücre çoğalması ve hayatta kalımının moleküler temellerini tanımlamaktı. Bu yaklaşımda, her bir hasta örneğinde tek seferde 20,000 genden her biri sistematik olarak susturuldu (işlevsiz hale getirildi). Böylece yapılan deneyde, bir genin susturulmasıyla, hücrelerde oluşan değişikler incelenerek, susturulan genin işlevinin ne olduğu anlaşılabilir. İki adet normal insan fetal nöral kök hücre kültüründeki paralel taramayla, glioblastoma kök hücre taramasının verileri karşılaştırıldı. Ayrı kemogenomik taramalar, TMZ’ye karşı tümör direnciyle ilişkili genleri ve potansiyel terapi stratejilerini tanımlamak için gerçekleştirildi.
Kanser kök hücreleri, tümör büyümesini teşvik eder ve hastalığın ilerlemesine neden olur. Bu hücreleri etkili şekilde hedefleyebilmek için, büyüme programlarını kontrol eden genlerin anlaşılması önemlidir. Hangi genlerin hayatta kalma ve çoğalma için gerekli olduğu bilinirse, bu genleri susturma ve tümör gelişimini durdurma yolları aranabilir.
Sonuçlar; glioblastoma gelişimi ve hayatta kalımı için, SOX gen ailesinin (SOCS3, USP8 and DOT1L) ve protein ufmylation yolağı genlerinin önemini vurguluyor. Yaygın GSC hayatta kalım genlerinin tanımlanması, hastalar arasındaki tümör çeşitliliğine rağmen, glioblastomanın biyolojisini anlamaya ve klinik öncesi değerlendirme yapabilmeye olanak tanıyacaktır.
10 GSC kültürünün sekizinde DOT1L, tümörün devamı için gerekli bulundu. Klinik öncesi modellerde ek çalışmalarda, Calgary Üniversitesi’nde, lösemi tedavisi için kullanılan bir ilacın, GSC’lerde DOT1L gen ürününü (proteinini) baskılayabildiğini gösterdi. Beyin kanserinde bu proteinin baskılanması, tümör gelişimini azalttı ve klinik öncesi modelde daha uzun süre hayatta kalmayı sağladı.
Bu taramalar; GSC gelişimi için önemli olan çok sayıda stres sinyal yolağını tanımladı. Önceki çalışmalarla birlikte, glioblastoma için JNK sinyalini hedefleyen tedavi edici stratejilerin etkinliğini destekliyor. Glioblastomada hastalar arasındaki farklılıklara rağmen, GSC gelişimi ve hayatta kalımı için yaygın mekanizmaların keşfi, daha geniş hasta grupları için kişiye özel terapi yöntemi geliştirmeye katkı sağlayabilir.
Araştırma grubu ayrıca, TMZ’e direnç ile ilgili genleri tanımlamak için, hastalardan türevli glioblastoma kültürlerinde ek CRISPR-Cas9 taraması 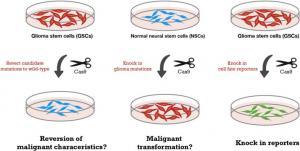 gerçekleştirdi. GSC kültürlerinde tüm genlerin korunmamış olmasına rağmen, bulgularda vurgulanan genler, Fanconi anemi yolağı (DNA onarımı ve kopyalanmasını içeren süreçle ilgili biyokimyasal yolak) ile ilişkiliydi.
gerçekleştirdi. GSC kültürlerinde tüm genlerin korunmamış olmasına rağmen, bulgularda vurgulanan genler, Fanconi anemi yolağı (DNA onarımı ve kopyalanmasını içeren süreçle ilgili biyokimyasal yolak) ile ilişkiliydi.
Özetle, hasta türevli GSC kültürlerinde CRISPR taraması, bir dizi genetik yatkınlığı ortaya çıkardı ve glioblastomada ilaç hedeflerinin tanımlanması için veri sağladı. Gelecek çalışmalar; hangi genlerin ve yolakların GSC hayatta kalımını ve kimyasallara duyarlılığını düzenlediğini ve hastalığın ilerleyişine katkıda bulunup bulunmadığını açıklayacaktır.
Kaynakça:
www.genengnews.com
Yazar: Ayça Olcay
