Çeşitli molekül ve iyonların protein yüzeyindeki belirli bölgelere bağlanma yeteneği, çok çeşitli protein fonksiyonlarının temelini oluşturur. Ligand, protein yüzeyine, zıt yüklü iyonik veya polar gruplarla polar olmayan bölgeler arasındaki van der Waals kuvvetleri ile bağlanan herhangi bir molekül veya iyondur. Bağlanma sahası ise, bir ligandın bağlandığı protein bölgesidir. Kimyasal özgüllük ve afinite, bir bağlanma bölgesinin farklı özellikleridir.
Kimyasal Özgüllük
Bir proteinin birden fazla bağlanma noktası olabilir, her site belirlenmiş bir ligand cinsine ya da liganda özgüdür. Bu yüksek kimyasal özgüllük, ligand ve proteinin tamamlayıcı şekillerinden kaynaklanmaktadır.
Benzeşme
Afinite, ligand-protein bağlanmasının gücüdür. Bir bağlanma sahası, her ikisindeki grupların doğasına ve birbirine yakınlığına bağlı olarak bir ligand için yüksek veya düşük afiniteye sahip olabilir.
Doyma
Tek bir bağlanma bölgesi işgal edilmiş veya kullanılmamış olabilir ve işgal edilen sitelerin fraksiyonuna doygunluk adı verilir. Doygunluk yüzdesi, bağlanmamış ligand konsantrasyonuna ve bağlanma bölgesinin afinitesine bağlıdır. Bu doygunluk, protein-ligand kompleksinin biyolojik aktivitesine yansıyacaktır.
Rekabet
Aynı bağlanma bölgesi için iki benzer ligand arasında bir rekabet varsa, birinin konsantrasyonundaki bir artış diğerinin bağlanmasını engelleyecektir.
Bağlayıcı Sitelerin Düzenlenmesi
Allosterik modülasyon
 Bir ligand modülatör molekülünün bir düzenleyici bölgeye kovalent olmayan bağlanmasıyla fonksiyonel (aktif) sahanın şeklinde bir değişiklik içerir. Modülasyon, bir kapatma veya açma işlevi şeklini alabilir. Multimerik bir proteinde, fonksiyonel gruplar arasındaki işbirliğine bağlı olarak ligand bağlanma afinitesinde bir artış olabilir. Bu süreç, oksijenin hemoglobine bağlanmasında meydana gelmektedir.
Bir ligand modülatör molekülünün bir düzenleyici bölgeye kovalent olmayan bağlanmasıyla fonksiyonel (aktif) sahanın şeklinde bir değişiklik içerir. Modülasyon, bir kapatma veya açma işlevi şeklini alabilir. Multimerik bir proteinde, fonksiyonel gruplar arasındaki işbirliğine bağlı olarak ligand bağlanma afinitesinde bir artış olabilir. Bu süreç, oksijenin hemoglobine bağlanmasında meydana gelmektedir.
Kovalent modülasyon
Bir kimyasal grup, daha çok, bir fosfat grubunun PO kovalent bağ ile işlevsel bir site şekil değişimini içeren bir fosforilasyon reaksiyonu ile etkilenmesidir.
Enzimler ve Kimyasal Reaksiyonlar
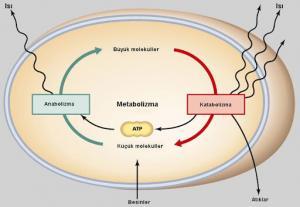
Metabolizma, hücre yapısı ve işlevi için gerekli olan organik moleküllerin sentezi (anabolizma) ve parçalanmasından (katabolizma) oluşmaktadır. Kimyasal reaksiyonlar reaktan moleküllerdeki kimyasal bağların kopması ve ürün molekülleri oluşturmak için yeni kimyasal bağların yapılmasını içermektedir. Kimyasal reaksiyonlar sırasında enerji ısı olarak eklenir veya açığa çıkmaktadır.
Reaksiyon Hızlarının Belirleyen Faktörler
Bir kimyasal reaksiyonun hızı (birim zamanda oluşan ürün moleküllerinin sayısı) aşağıdakilerden etkilenir:
• Reaktif konsantrasyonu: Reaktan ne kadar fazlaysa, oran o kadar yüksek olur.
• Aktivasyon enerjisi: Reaktan moleküllerin kimyasal bağların kırılıp oluşabileceği aktif hale gelmek için ihtiyaç duyduğu enerjidir. Gereken aktivasyon enerjisi ne kadar yüksekse, reaksiyon hızı o kadar düşüktür.
• Sıcaklık: Sıcaklık ne kadar yüksek olursa reaksiyon hızı o kadar yüksek olur çünkü reaktan moleküller gerekli aktivasyon enerjisini elde edebilir.
• Katalizör: Reaksiyon hızını artırmak için gerekli aktivasyon enerjisini azaltan bir madde. Bir katalizörün kimyasal bileşimi reaksiyonla değişmez ve bu nedenle tek bir katalizör molekülü defalarca kullanılabilir.
Bir Reaksiyonun Tersinirliği
Bir reaksiyon sırasında açığa çıkan enerji, bir reaksiyonun tersine çevrilebilirliğini belirler. Bir reaksiyon sırasında salınan enerji ne kadar büyük olursa, ürün moleküllerinin bu enerjiyi elde etme ve reaktanları yeniden oluşturmak için ters reaksiyona girme olasılığı daha düşüktür. Böyle bir durumda, ürünün reaktan konsantrasyonuna oranı büyük olacak ve reaksiyon geri döndürülemez olma eğiliminde olacaktır. Tersine çevrilebilir bir kimyasal reaksiyonda, kimyasal denge adı verilen bir durumda eşit olana kadar reaksiyon ilerledikçe ileri reaksiyon hızı azalır ve ters reaksiyon hızı artar, bu noktada reaktanların konsantrasyonunda daha fazla değişiklik olmaz.
Kitle Eylem Yasası
Reaktant ve ürün konsantrasyonunun net reaksiyon yönüne etkisi. Reaktanların konsantrasyonunun arttırılması veya ürünlerin konsantrasyonunun azaltılması, reaksiyonu ileri doğru iter ve bunun tersi de geçerlidir. Bu mekanizma, metabolik yolların yönünü kontrol etmede önemlidir.
Enzimler
Protein katalizörleri
Birkaç RNA molekülü de katalitik aktiviteye sahiptir. Enzim aracılı bir reaksiyonda, bir enzim, ürünleri ve enzimi salmak üzere parçalanan bir enzim-substrat kompleksi oluşturmak için reaktanlara (substratlar) bağlanırlar. Sübstratın bağlandığı enzim bölgesi, şekli enzimin kimyasal özgüllüğünü belirleyen aktif bölge olarak adlandırılır.
Kofaktörler
Konformasyonlarını değiştirmek ve onları aktif hale getirmek için enzimlere bağlanan maddelerdir. Bazı kofaktörler iz elementlerdir. Kofaktörün organik bir molekül olduğu durumlarda buna koenzim denir. Koenzimler vitaminlerden elde edilir.
Enzim aracılı reaksiyonların düzenlenmesi
Enzim aracılı bir reaksiyonun hızı şunlara bağlıdır:
• Substrat konsantrasyonu : Substrat konsantrasyonu ne kadar yüksekse, enzim doyana kadar reaksiyon hızı o kadar yüksek olur. Substrat konsantrasyonu, diyetteki değişiklikler, bağırsaktan emilim hızı, plazma membranının geçirgenliğindeki değişiklikler veya hücre içi parçalanma ve maddenin sentezindeki değişiklikler nedeniyle bir hücrenin dışından tedarikteki değişikliklerle değişir.
• Enzim konsantrasyonu: Enzim konsantrasyonu ne kadar yüksekse reaksiyon hızı o kadar yüksek olur.
• Enzim aktivitesi: Bir enzimin aktivitesi, bağlanma sahası afinitesinin allosterik veya kovalent modülasyonu ile değiştirilebilir. Modülatörler, diğer kimyasal reaksiyonların ürünleridir veya kimyasal sinyallerle etkinleştirilir.
Çok enzimli metabolik yollar
Enzim aracılı reaksiyonlar dizisidir. Genel olarak, tüm yolun hızını düzenleyen dizideki en yavaş adım olan hız sınırlayıcı bir reaksiyondan oluşur. Bu adımı kontrol eden enzim, genellikle son ürün inhibisyonu veya yolun son ürünü tarafından inhibisyon ile güçlü bir şekilde düzenlenir.
ATP
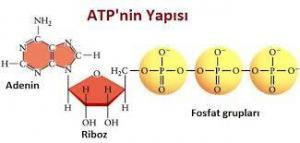 Adenozin trifosfat, yakıt moleküllerinin, karbonhidratların ve yağların parçalanması sırasında enerjinin aktarıldığı birincil moleküldür. (Bir hücre, işlevlerini yerine getirmek için ısı enerjisini kullanamaz). ATP daha sonra kuvvet ve hareket üretimi, zarlar arasında aktif taşıma ve hücre yapılarında kullanılan organik moleküllerin sentezi gibi fonksiyonlarda, hücrelerde enerji gerektiren süreçler tarafından kullanılabilen enerjiyi serbest bırakmak için hidrolize edilir. ATP bir enerji transfer molekülüdür ve bir enerji depolama molekülü DEĞİLDİR. Enerjiyi yakıt moleküllerinden hücrelere küçük miktarlarda aktarır.
Adenozin trifosfat, yakıt moleküllerinin, karbonhidratların ve yağların parçalanması sırasında enerjinin aktarıldığı birincil moleküldür. (Bir hücre, işlevlerini yerine getirmek için ısı enerjisini kullanamaz). ATP daha sonra kuvvet ve hareket üretimi, zarlar arasında aktif taşıma ve hücre yapılarında kullanılan organik moleküllerin sentezi gibi fonksiyonlarda, hücrelerde enerji gerektiren süreçler tarafından kullanılabilen enerjiyi serbest bırakmak için hidrolize edilir. ATP bir enerji transfer molekülüdür ve bir enerji depolama molekülü DEĞİLDİR. Enerjiyi yakıt moleküllerinden hücrelere küçük miktarlarda aktarır.
Metabolik Yollar
Glikoliz
Başta glikoz olmak üzere karbonhidratları kısmen katabolize eder. 6 C glikozu iki 3 C piruvata dönüştürür ve substrat seviyesinde fosforilasyon adı verilen bir işlemle net 2 ATP kazancı sağlar. Reaksiyonlar oksijen kullanmaz ve sitozolde gerçekleşir. Oksijen varsa (aerobik koşullar), piruvat Krebs döngüsüne girer. Oksijen yokluğunda (anaerobik koşullar), piruvat laktata dönüştürülür. Glikoliz, mitokondriya sahip olmayan hücrelerde, örneğin eritrositlerde ve yoğun kas aktivitesi sırasında belirli iskelet kası hücrelerinde meydana gelir. Fruktoz ve galaktoz gibi diğer monosakkaritler de glikoliz ile katabolize edilebilir. Bazı organizmalarda, örneğin maya, piruvat CO dönüştürülür ve buna fermentasyon adı verilir.
Krebs döngüsü
Sitrik asit döngüsü veya trikarboksilik döngü olarak da adlandırılır. Karbonhidrat, protein veya yağ parçalanması sırasında üretilen molekülleri kullanır ve CO 2 üretir, hidrojen koenzimlere ve 1 ATP’ye bağlıdır. Reaksiyonlar mitokondriyal matrikste meydana gelir ve oksijen kullanır. Döngüye giren birincil molekül, piruvat, yağ asitleri veya amino asitlerden türetilen asetil koenzim A’dır (asetil CoA). Toplam ATP üretimi 2’dir, çünkü 2 piruvat molekülü, glikolizden döngüye girmektedir.
Oksidatif fosforilasyon
Oksidatif fosforilasyon, Krebs döngüsünden koenzimlere bağlanan hidrojeni ve oksijeni su ve 34 ATP molekülü üretmek için kullanır ve bu süreçte koenzimlerin hidrojensiz formunu serbest bırakır. Sitokromların aracılık ettiği iç mitokondriyal membranda meydana gelen sürece elektron taşıma zinciri de denir.
Karbonhidrat Sentezi
Glikojen depolama
Glikoz, iskelet kaslarında ve karaciğerde bir polisakkarit olan glikojen formunda depolanır. Glikojen sentezi ve parçalanması için enzimler sitozolde bulunur. Glikozun piruvat oluşturmak için katabolik yola girip girmediği veya glikojen oluşturmak için anabolik yola girip girmediği, tek bir noktada kontrol edilir. Ve enzimleri modüle eden hormonlar tarafından çalıştırılan bir geri bildirim mekanizması altında çalışır.
Glikoz sentezi
Glikoz, karaciğerde ve böbreklerde gliserol ve bazı amino asitlerin katabolizmasından türetilen ara maddelerden, glukoneogenez adı verilen bir işlemle sentezlenir. Bu süreçteki ana substrat piruvattır ve 1 molekül glikoz üretmek için 6 ATP molekülü tüketilir.
Yağ Metabolizması
Yağ katabolizması
Beta oksidasyon adı verilen bir dizi reaksiyonla, mitokondriyal matrikste meydana gelen yağ asitlerinin katabolizmasından önemli miktarda enerji elde edilir. Asetil CoA üretilir ve daha sonra Krebs döngüsüne girebilir. Bir 18 C doymuş yağ asidinin katabolizması 146 ATP verir.
Yağ sentezi
Yağ, vücutta depolanan enerjinin büyük bir bölümünü oluşturur. Asetil CoA molekülleri uzun, çift sayılı C zincirleri oluşturmak için bir araya gelir ve bu yağ asitleri, pürüzsüz endoplazmik retikulumda triaçilgliseroller oluşturmak için gliserollerle birleşir. Vücut yağının çoğu, tüm sitoplazması tek bir yağ damlasıyla dolu olan adiposit adı verilen hücrelerde depolanır. Adipositler, besin alımı sırasında triasilgliserolleri sentezler ve depolar ve çoğu derinin altında bulunan adipoz dokusu oluşturmak için kümelenir.
Protein ve Amino Asit Metabolizması
Amino asit katabolizması
Protein katabolizması, peptit bağlarını kırmak ve daha küçük peptitleri veya amino asitleri serbest bırakmak için proteazları gerektirir. Amino asitler, ATP oluşturmak veya çeşitli başka moleküller için ara ürünler sağlamak üzere katabolize edilebilir. Amino asidin amino grubu ya da bir keto asit elde etmek için oksidatif deaminasyon uzaklaştırılmıştır ve NH olduğu 3 ya da transaminasyon bir keto aside aktarılır. Keto asit, glikolitik yola veya glikoz ve yağ için sentetik yollara girebilir. Amino grubundan N, pürinler ve pirimidinler gibi önemli N içeren molekülleri sentezlemek için kullanılabilir. Toksik NH 3 plazma membranı vasıtasıyla kana geçer ve böbrekler tarafından atılır nispeten toksik olmayan üre oluşturulması için CO2 ile bağlantılıdır karaciğer gider.
Amino asit sentezi
 Keto asitler, örneğin piruvik asit, amino asitler oluşturmak için transamine edilebilir. Bu işlem 20 amino asitten sadece 11’ini oluşturabilir ve besinlerden elde edilmesi gereken kalan 9’a esansiyel amino asitler denir. Vücuttaki toplam serbest amino asit havuzları şunlardan elde edilir:
Keto asitler, örneğin piruvik asit, amino asitler oluşturmak için transamine edilebilir. Bu işlem 20 amino asitten sadece 11’ini oluşturabilir ve besinlerden elde edilmesi gereken kalan 9’a esansiyel amino asitler denir. Vücuttaki toplam serbest amino asit havuzları şunlardan elde edilir:
• Sindirim sırasında alınan protein amino asitlere indirgenir,
• Keto asitlerden gerekli olmayan amino asitlerin sentezi
• Vücut proteinlerinin parçalanması
Bunlar, proteinlerin sentezlenebileceği havuzlardır.
Temel Besinler
Temel besinler, vücudun optimal işlevi için gerekli olan ancak hiç sentezlenemeyen veya vücut tarafından sadece yetersiz miktarlarda sentezlenebilen maddelerdir. Sürekli olarak yiyecek olarak tedarik edilmeleri gerekir. Su temel bir besindir çünkü idrarda, ciltte ve solunum yollarında vücut tarafından sentezlenebileceğinden çok daha fazlası kaybolur. Mineral elementler, 9 temel amino asit, iki yağ asidi, linoleik ve linolenik asitler, inositol, kolin ve karnitin temel besin maddeleridir.
Vitaminler
Vitaminler, küçük miktarlarda gerekli olan 14 organik temel besin grubudur. Bitkiler ve bakteriler, vitamin sentezlemek için enzimlere sahiptir ve bunlar birincil vitamin kaynaklarıdır. Suda çözünen fazla vitaminler idrarla atılırken, yağda çözünenler yağ dokusunda depolanır.
Kaynakça:
https://www.nature.com/scitable/topicpage/cell-metabolism-14026182
https://www.biologyonline.com/tutorials/protein-activity-and-cellular-metabolism#:~:text=Metabolism%20consists%20of%20synthesis%20(anabolism,bonds%20to%20form%20product%20molecules.
Yazar: Özlem Güvenç Ağaoğlu
