Son 5 yılda hayatta kalma oranını artırabilecek ve mortalite oranını azaltabilecek birkaç yeni strateji eklenmiştir; miRNA tedavisi bu stratejilerden biridir. Kanser için miRNA azaltma veya inhibisyon terapisi ve kanser için miRNA replasman veya restorasyon terapisi olmak üzere iki miRNA bazlı tedavi yaklaşımı bulunmaktadır.
miRNA Replasman veya Restorasyon Tedavisi
miRNA replasman veya restorasyon terapisi, kanserlerde silinen veya aşağı regüle edilen miRNA’ların yeniden kullanılmasını kullanmaktadır. Bu konuda bazı çalışmalar yapılmıştır. Bonci ve ark, Prostat kanseri hücre dizilerinde miRNA’yı tanıtmışlardır. Prostat kanseri hücre hatlarında miR-15a ve miR-16-1 kümeleri kullanmışlardır; burada çok sayıda onkojenik aktiviteyi hedefleyerek apoptozu indüklemişlerdir, proliferasyonu bloke etmişlerdir ve prostat kanserini kontrol etmişlerdir. Trang ve ark., MiR-34a ve let-7 kullanılarak tümör baskılayıcı miRNA’ların sistemik olarak verilmesini gerçekleştirmişlerdir. Bu yaklaşım, KRAS (K-ras; bir proto-onkogen) ile aktifleştirilmiş küçük hücreli dışı akciğer kanseri fare modelinde tümör yükünü azaltmıştır.
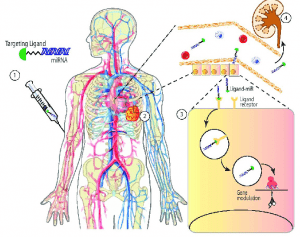 Tümör dokusunda biriken miR-34a, bunu doğrudan hedeflerinin aşağı regülasyonu izlemiştir. Bu nihayetinde tümör alanında % 60’lık bir azalmaya neden olmuştur. Burada, araştırmacılar, lipit bazlı dağıtım aracını kullanmışlardır, böylece miRNA (miR-34a veya let-7 mimik), bir lipit süspansiyonu ile bir kompleks oluşturmuştur. Başka bir çalışmada, Tazawa ve arkadaşları MiR-34a ve miR-16’nın sistemik verilmesini gerçekleştirmiş, prostat ve kolon kanseri gelişimini başarılı bir şekilde bastırmıştır. Araştırmacılar bir KRAS mutant fare modelinde let-7a’nın adenovirüs ekspresyonunu kullanmışlardır. Bu çalışmalarda, araştırmacılar bir ksenograft fare modelinde veya faregiller akciğer tümörü modelinde akciğer kanserinin büyümesini etkili bir şekilde kontrol etmişlerdir. İlk ticari miRNA restorasyon tedavisi MRX34’tür. Bu MRX34, intravenöz olarak enjekte edilebilen lipozom bazlı bir miR-34 mimikidir. Halen ileri hepatoselüler karsinom hastaları için Faz I klinik çalışmalarında araştırılmaktadır.
Tümör dokusunda biriken miR-34a, bunu doğrudan hedeflerinin aşağı regülasyonu izlemiştir. Bu nihayetinde tümör alanında % 60’lık bir azalmaya neden olmuştur. Burada, araştırmacılar, lipit bazlı dağıtım aracını kullanmışlardır, böylece miRNA (miR-34a veya let-7 mimik), bir lipit süspansiyonu ile bir kompleks oluşturmuştur. Başka bir çalışmada, Tazawa ve arkadaşları MiR-34a ve miR-16’nın sistemik verilmesini gerçekleştirmiş, prostat ve kolon kanseri gelişimini başarılı bir şekilde bastırmıştır. Araştırmacılar bir KRAS mutant fare modelinde let-7a’nın adenovirüs ekspresyonunu kullanmışlardır. Bu çalışmalarda, araştırmacılar bir ksenograft fare modelinde veya faregiller akciğer tümörü modelinde akciğer kanserinin büyümesini etkili bir şekilde kontrol etmişlerdir. İlk ticari miRNA restorasyon tedavisi MRX34’tür. Bu MRX34, intravenöz olarak enjekte edilebilen lipozom bazlı bir miR-34 mimikidir. Halen ileri hepatoselüler karsinom hastaları için Faz I klinik çalışmalarında araştırılmaktadır.
miRNA Azaltma veya İnhibisyon Tedavisi
miRNA azaltma veya inhibisyon tedavisi, kanserlerde, özellikle tümörlerde aşırı eksprese edilen veya yukarı regüle edilen miRNA’ları etkisiz hale getirebilmektedir. Birkaç miRNA inhibe edici ajan zamanla incelenmiştir. Bazıları kilitli nükleik asit veya LNA, antisens anti-miR oligonükleotitler, miRNA’ların küçük molekül inhibitörleri ve miRNA süngerleridir. LNA bir nükleik asit analogudur ve LNA, bir veya daha fazla nükleotit monomerden oluşabilmektedir. Anti-miRNA oligonükleotitler (AMO’lar) (2′-O-metil AMOlar ve 2′-O-metoksietil) LNA anti-miR’lerdir.
Bu LNA durumunda, 2-O ve 4-C atomlarını bağlayan ek bir metilen köprüsü vardır ve bu riboz halkasını kilitlemektedir. Bu belirli bölgede bir C3′-endo veya C2′-endo konformasyonu görülebilmektedir. LNA durumunda Watson-Crick’in hedef mRNA’lara bağlanması yüksek bir afinite olabilmektedir. Elmén ve arkadaşları, insan olmayan primatlarda LNA aracılı miRNA susturma gerçekleştirmişlerdir. Primat modellerinde LNA-anti-miR intravenöz enjeksiyonlar sağlamışlardır, yani sitoplazmada LNA-anti-miR alımına neden olan Afrika yeşil maymunları. LNA-anti-miR ve miR-122’yi bağlayan bir heterodupleks konfigürasyonu oluşturmuşlardır. Sharifi ve Salehi miR-92a-3p’yi LNA-anti-miR92a-3p ile bloke etmiştir. Bu LNA inhibisyonu apoptozu teşvik etmiş ve insan akut lösemisinde hücre yayılmasını durdurmuştur. Ticari LNA-anti-miR, Santaris Pharma tarafından yürütülen bir klinik araştırmaya girmiştir. Bir LNA-anti-miR-122 olan Miravirsen, Faz I ve IIa klinik çalışmalarında tahmin edilen verime sahiptir. Bu LNA-anti-miR, hepatit C virüsünü (HCV) yönetmek için kullanılmıştır.
Birkaç küçük molekülün miRNA’ları inhibe ettiği bildirilmektedir. 2008 yılında, Gumi reddy ve ark, MiR-21’in küçük moleküllü inhibitörleri (SMIR’ler) rapor etmiştir. Bu çalışmada, olası miRNA’ya özgü küçük molekül inhibitörlerinin kullanıldığı büyük ölçekli ilaç taramasını tanımak için lusiferaz bazlı bir raportör analizi de geliştirilmiştir. Naro ve ark, MiR-21’in aril amid küçük moleküllü inhibitörleri gibi yeni bir tür küçük molekül inhibitörleri hakkında rapor vermiştir. Bu miRNA, farklı insan kanser türlerinde ve HeLa hücrelerinde aşırı eksprese edilmiştir ve miRNA süngerleri, çoklu tandem tekrarlı RNA transkriptlerine sahip miRNA’yı antagonize etmektedir. Sünger RNA’larının bir miRNA’nın karşısındaki bağlanma yerlerini kapsadığı kaydedilmiştir.
Liang ve arkadaşları, kolorektal kanserde miRNA süngerleri olarak işlev gören lncRNA H19 gibi uzun kodlama yapmayan RNA (lncRNA) geliştirmişlerdir. Ma ve ark, aşırı malign hücrelerde miR-9’u engelleyebilen bir miRNA süngeri geliştirmişlerdir. Bu sünger, metastaz gelişimini yavaşlatan murin modellerinde pulmoner mikro metastazda kullanılmaktadır. miR-9 yoğunluğu MYCN amplifikasyonu, metastatik durum ve tümör sıralaması ile bağlantılıdır.
MiRNA Terapötikleri ile İlgili Zorluklar
MiRNA tabanlı terapötiklerin geliştirilmesinde bazı zorluklar vardır ve İn vivo düşük RNA stabilitesi kaydedilmiştir. RNA’nın yarı ömrü miRNA tedavisi ile artmaktadır. Diğer bir karmaşıklık, tümöre özgü miRNA’ların verilmesi ve tutulmasıdır. miRNA’lar aynı zamanda bir meydan okuma olan çok sayıda mRNA’yı hedeflemektedir. Bazen, hedeflenen verme molekülleri, karaciğer ve böbrekler gibi organlara verilen küçük moleküllerin hızlı lokalizasyonu ile ilk geçiş metabolizmasında sıkışabilmektedir. Bununla birlikte, nanoparçacık iletimi sorunu çözebilmektedir, 15 ila 100 nm arasında değişen nanopartiküller, miRNA’nın hedefe özgü dağıtımını kolaylaştıran sistemik uygulama için en iyi boyuttur.
Kemoterapötik Ajanlarla Kombinasyon Tedavisi
 Kanser tedavisinde kombinasyon tedavisi kullanılmaktadır. İlk başarılı kemoterapi kombinasyonu akut çocukluk çağı lösemisini tedavi edebilmektedir ve daha sonra Hodgkin hastalığını tedavi etmek ve ileri kanserleri tedavi etmek için genişletilmiştir. Akut çocukluk çağı lösemisini tedavi etmek için bir POMP kemoterapi rejimi ve tersine, lenfoma tedavisinde MOPP kemoterapi rejimi kullanılmıştır. Ayrıca, rasyonel ilaç kombinasyonları, tümör metastazını azaltmada büyük umut vaat ederek, birden fazla tümör hücresi sağkalım yoluna müdahale etmeye yardımcı olabilmektedir. İlaç kombinasyonlarının kullanılmasından bu yana, ulusal kanser oluşumu ve mortalitesi 1990 yılında düşmeye başlamıştır. Kanser mortalitesi yaşlanan ABD nüfusuna rağmen her yıl azalmaya devam etmektedir
Kanser tedavisinde kombinasyon tedavisi kullanılmaktadır. İlk başarılı kemoterapi kombinasyonu akut çocukluk çağı lösemisini tedavi edebilmektedir ve daha sonra Hodgkin hastalığını tedavi etmek ve ileri kanserleri tedavi etmek için genişletilmiştir. Akut çocukluk çağı lösemisini tedavi etmek için bir POMP kemoterapi rejimi ve tersine, lenfoma tedavisinde MOPP kemoterapi rejimi kullanılmıştır. Ayrıca, rasyonel ilaç kombinasyonları, tümör metastazını azaltmada büyük umut vaat ederek, birden fazla tümör hücresi sağkalım yoluna müdahale etmeye yardımcı olabilmektedir. İlaç kombinasyonlarının kullanılmasından bu yana, ulusal kanser oluşumu ve mortalitesi 1990 yılında düşmeye başlamıştır. Kanser mortalitesi yaşlanan ABD nüfusuna rağmen her yıl azalmaya devam etmektedir
Kemoterapi tedavi programlarında kombinasyon terapisi ile kayda değer başarıya rağmen, kemoterapötik tedaviye direnç etkili tedaviye bir zorluk olarak ortaya çıkmıştır. Birçok kanser türünün kemoterapiye duyarlı olduğu kaydedilmiştir; zamanla kanser hücreleri, DNA mutasyonları ve ilaçları inhibe eden ve parçalayan metabolik değişiklikler gibi farklı mekanizmalarla direnç geliştirebilmektedir. Günümüzde, çeşitli miRNA’larla kemoterapötik ajanlarla birlikte kombinasyon terapisi kavramı, sinerjistik etkiler sağlayarak kanser hastalarına yardımcı olabilmektedir. HCV tedavisi için bu tip bir kombinasyon terapisi bir Faz II klinik çalışmasında değerlendirilmektedir. Bu durumda, bir miRNA, HCV tedavisinde telaprevir ve ribavirin gibi antiviral ilaçlarla kullanılan anti-miR’dir.
MiRNA Tabanlı Kemo-Kombinasyon Terapilerinin Mantığı
Kemoterapötik ilaçlara karşı direnç vardır ve kemoterapötik direnç raporları gün geçtikçe artmaktadır. Kemoterapiden sonra aktif olmaya devam eden kemo-dirençli kanser hücrelerinin tümör nüksünden sorumlu olduğu öne sürülmüştür. Bununla birlikte, kanser hücrelerinin kemo-direnç geliştirdiği mekanizmaları anlamamız gerekmektedir. Tümör hücrelerinin kemo/ilaç direnci geliştirme olasılığının daha yüksek olduğu bazı anahtar mekanizmalar önerilmiştir; bunlar kemoterapide akıntı pompa aracılı direnci ve kemoterapide akıntı olmayan pompa aracılı direnci içermektedir.
Kemoterapide Akış Pompa Aracılı Direnç
Akış pompaları tüm hücrelerde bulunmaktadır ve hücreleri kimyasal toksisiteden, özellikle organik kimyasal toksisiteden korumaktadır. Prokaryotik ve ökaryotik hücrelerde enerjiye bağımlı bir ilaç akış pompasıdır. Bununla birlikte, kanser hücrelerinde, MDR-1 geninin, esas olarak, akıntı pompasını tetiklemekten sorumlu olduğu gözlenmiştir. Benzer şekilde, MDR-1a ve MDR1b gibi dışarı akış pompasının tetiklenmesinde başka bazı genler de yer almaktadır. P-glikoprotein, MDR1 genine bağlıdır ve bu gen kanser hücrelerinde aşırı eksprese edildiğinde, kanser kemoterapi direncine katkıda bulunmaktadır. Sitotoksisite, antikanser ajanların plazma konsantrasyonunu arttıran sitokrom P-450 enzimlerinin inhibisyonundan kaynaklanmaktadır ve son olarak, akış pompaları bastırılmaktadır. ATP bağlayıcı kaset (ABC) taşıyıcı aile protein üyeleri, akış pompalarını mümkün kılmaktadır ve sağlıklı hücrelerin plazma zarlarında bulunmaktadır. ABC taşıyıcı normal fizyolojik sürecin bir parçasıdır ve P-glikoprotein çıkış pompaları ABC taşıyıcı aile proteininin ilk üyelerinden biridir.
P-glikoproteinle ilişkili akış pompaları genellikle hücre zarında ve bunlar nükleer zarda bulunmaktadır. Bu P-glikoprotein ile ilişkili akış pompaları, pozitif veya nötr olarak yüklü moleküllere bağlanma kapasitesine sahiptir. Araştırmacılar çoğu kemoterapötik ilacın tarafsız veya hücresel pH altında pozitif yüklü olduğunu bildirmiştir. Bu nedenle kemoterapötik ilaçlar, P-glikoproteinle ilişkili akış pompaları için bir substrat görevi görür ve kemoterapötik ilaçlar hücreden dışarı pompalanabilmektedir.
Kemoterapide Akmayan Pompa Aracılı Direnç
Kemoterapide akıntı olmayan pompa aracılı direnç, ilaç inaktivasyonu, ilaç hedeflerinin değiştirilmesi, DNA hasar onarımı, hücre ölümünün inhibisyonu, vb. İle ilgilidir. Housman ve arkadaşları, elo olarak tarif edilen ilaç inaktivasyonu, ilaç hedeflerinin değiştirilmesi, DNA hasar onarımı, hücre ölüm inhibisyonu, vb. Rueff ve Rodrigues, genetik açıdan kanser ilacı direncini tanımlamışlardır. Bunlar, yukarı akış veya aşağı akış efektörleri olarak işlev görebilen bozulmuş miRNA düzeylerini tarif etmişlerdir. Aynı araştırmacılar ayrıca, hedeflenen tedavide ilaç hedeflerinin mutasyonunun yanı sıra kontrol noktalarında, hücre döngüsünde ve tümör mikro-ortamındaki değişiklikler hakkında da rapor vermişlerdir.
Mirna’nın Kanser Tedavisi İçin Kemoterapötik Ajanlarla Kombinasyon Tedavisi
 Kanserin tedavisi için çeşitli tipte kemoterapötik ajanlarla birlikte çeşitli miRNA tipleri ile farklı kombinasyon terapisinin kullanıldığı rapor edilmiştir. Gemsitabin, bir deoksisitidin analogu olan yeni bir antikanser nükleosididir. Gemsitabinin klinik etkinliği, kemo-direnci ve hızlı plazma metabolizması nedeniyle kanserde yavaşlamıştır. Tümör baskılayıcı miRNA-205, pankreas kanserini tedavi etmek için gemsitabin ile kombinasyon halinde kullanılmıştır. Bu modelde gemsitabin ile konjüge edilmiş katyonik kopolimer iletimi miR-205 ile gerçekleştirilmiştir. Gemsitabine dirençli pankreas kanseri hücrelerinde (MIA PaCa-2 (R) ve CAPAN-1 (R) hücreleri) tümör büyümesinde önemli bir inhibisyon kaydedilmiştir. Ayrıca Paklitaksel (PTX) farklı kanser türlerini tedavi etmek için kullanılan yeni bir antikanser ajandır. Marka adı, intravenöz tedavi olarak verilen Taxol’dur. Shi ve ark, MiR-34a ve paklitaksel kullanarak bir birlikte verme sistemi geliştirmişler ve bu kombinasyon terapisinin kanser tedavisi için sinerjistik etkilerini değerlendirmişlerdir. Bu sistemde miR-34a, katyonik olan katı lipit nanoparçacıklarda (miSLNs-34a/PTX) paklitaksel ile birlikte entegre edilmiştir. Bu birlikte taşıma sistemi, farelerde anti-kanser aktivitesini geliştirmiştir, tümör büyümesini önleme ve kanser hücresi popülasyonlarını kaldırma konusunda önemli bir potansiyele sahiptir.
Kanserin tedavisi için çeşitli tipte kemoterapötik ajanlarla birlikte çeşitli miRNA tipleri ile farklı kombinasyon terapisinin kullanıldığı rapor edilmiştir. Gemsitabin, bir deoksisitidin analogu olan yeni bir antikanser nükleosididir. Gemsitabinin klinik etkinliği, kemo-direnci ve hızlı plazma metabolizması nedeniyle kanserde yavaşlamıştır. Tümör baskılayıcı miRNA-205, pankreas kanserini tedavi etmek için gemsitabin ile kombinasyon halinde kullanılmıştır. Bu modelde gemsitabin ile konjüge edilmiş katyonik kopolimer iletimi miR-205 ile gerçekleştirilmiştir. Gemsitabine dirençli pankreas kanseri hücrelerinde (MIA PaCa-2 (R) ve CAPAN-1 (R) hücreleri) tümör büyümesinde önemli bir inhibisyon kaydedilmiştir. Ayrıca Paklitaksel (PTX) farklı kanser türlerini tedavi etmek için kullanılan yeni bir antikanser ajandır. Marka adı, intravenöz tedavi olarak verilen Taxol’dur. Shi ve ark, MiR-34a ve paklitaksel kullanarak bir birlikte verme sistemi geliştirmişler ve bu kombinasyon terapisinin kanser tedavisi için sinerjistik etkilerini değerlendirmişlerdir. Bu sistemde miR-34a, katyonik olan katı lipit nanoparçacıklarda (miSLNs-34a/PTX) paklitaksel ile birlikte entegre edilmiştir. Bu birlikte taşıma sistemi, farelerde anti-kanser aktivitesini geliştirmiştir, tümör büyümesini önleme ve kanser hücresi popülasyonlarını kaldırma konusunda önemli bir potansiyele sahiptir.
Doksorubisin (DOX), farklı kanser türlerini tedavi etmek için kullanılan kemoterapötik bir ilaçtır. Ticari isimlerinden biri Adriamisin’dir. MiR-34a gibi bir miRNA’nın antikanser aktivitesi bulunmaktadır. MiR-34a verilmesinin prostat kanseri metastazını ve progenitör hücrelerini inhibe ettiği bulunmuştur. CD44’ü baskılayarak prostat kanseri metastazını güçlü bir şekilde engellemektedir. Deng ve ark, Hiyalüronik asit-kitosan nanoparçacıkları kullanarak, nanopartiküllere yetkin bir şekilde kapsüllenmiş ve tümör hücrelerine veya tümör dokularına verilen miR-34a ve DOX’un birlikte verilmesini gerçekleştirmiştir. Bu iletim sisteminde, DOX-miR-34a birlikte yüklü hiyalüronik-kitosan nanopartikülleri, iyonotropik jelasyon yöntemi ile etkili bir şekilde düzenlenmiştir. Kombinasyon ilacının (DOX-miR-34a), bir anti-apoptoz geni, Bcl-2’nin ekspresyonunu sınırlandırarak anti-tümör aktivitesini arttırdığı gösterilmiştir.
Ayrıca Florourasil (5-FU) farklı kanser türlerini tedavi etmek için kullanılan yeni bir antikanser ajandır. Marka adı, intravenöz tedavi olarak verilen Adrucil’dir. 5-FU direnci nadiren görülür ki bu kanser yönetimi başarısızlığının ana nedenidir. MiR-129, anti-apoptotik bir protein olan B hücresi lenfoma-2’yi (Bcl-2) bastırarak apoptozu aktive eden antikanser miRNA aktivitesine sahiptir. Karaayvaz ve ark, bu miRNA’nın kolorektal tümör fare modelinde 5-FU sitotoksisitesini arttırdığını bildirmişlerdir. Kim ve arkadaşlarının bir başka çalışmasında, meme kanseri hücrelerini in vitro tedavi etmek için kullanılan adenoviral olarak yapılandırılmış bir miR-145 geliştirilmiştir.. Öte yandan, ortotopik fare meme kanseri modelini in vivo tedavi etmek için aynı bileşik (adenoviral yapılı miR-145 veya Ad-miR-145) kullanılmıştır.
Adenoviral yapılan miR-145’in, hem meme kanseri hücrelerinde hem de meme kanseri fare modelinde hücre büyümesini ve motilitesini baskıladığı bulunmuştur. Bu adenoviral yapılı miR-145, sadece 5-florourasil tedavisine göre antitümör etkilerini önemli ölçüde arttıran 5-florourasil ile kombinasyon halinde kullanılmıştır.
Dosetaksel (DTX) benzersiz bir geniş spektrumlu kemoterapötik ajandır. Özellikle katı kanserler olmak üzere farklı kanser türlerini tedavi etmek için kullanılmaktadır. Hermeking (2010) miRNA-34a’nın güçlü bir tümör baskılayıcı olduğunu tarif etmiştir. Son zamanlarda nanokarrier, metastatik meme kanserini tedavi etmek için hem DTX hem de miRNA-34a molekülünü vermek için kullanılmıştır. Bu durumda, terapötik moleküllerin kombinasyonunu vermek üzere katyonik albümin ile kaplanan bir nanokariyer çekirdek kabuğu hazırlanmıştır. Her iki molekülün (dosetaksel ve miRNA-34a) birlikte verilmesinin, metastatik meme kanserini tek başına dosetaksel veya miRNA-34a’ya kıyasla etkili bir şekilde tedavi edebildiği gözlenmiştir.
Kaynakça:
https://www.oncotarget.com/article/24309/text/
https://www.frontiersin.org/articles/10.3389/fendo.2018.00402/full
https://www.sciencedirect.com/science/article/pii/S2451965020300077
https://www.nature.com/articles/nrg3965
Yazar: Özlem Güvenç Ağaoğlu
