Nörodejeneratif hastalıklarda gözlenen hücre ölümü modlarını tanımlayan ölüm sonrası hasta dokusunda artan kanıtlar vardır. Bu tür kanıtların, çoğu nörodejeneratif hastalığın uzun süreli doğasından dolayı birikmesi zor olmuştur, böylece tüm hücre popülasyonunun sadece küçük bir kısmı herhangi bir zamanda ölme sürecindedir. Hücre ölümü uzun yıllar boyunca meydana geldiğinden, bu tür numunelerden elde edilen anlık çekim temsili sadece son zamanlarda ölen hücreleri ortaya çıkarabilmektedir. Genellikle bu dokular, hastalığın son aşamasını temsil etmektedir, nöronal hücre ölümünü önlemeye çalışmak için bu tür hastaları ideal olarak tedavi etmek istenilen zamandan itibaren uzaklaştırılmaktadır.
Genellikle ölmekte olan ve ölü hücreler karışık sinyaller göstermektedir ve sınıflandırmayı farklı hücre ölümü modellerine karşı koymaktadır. Hasta örnekleriyle ilgili bir başka zorluk, farklı hücre ölümü modları için kullanılan belirteçlerin örtüşen, spesifik olmayan ve bu nedenle yanlış yorumlanmaya eğilimli olabilmesidir. Örneğin, terminal transferaz dUTP nick-end etiketleme (TUNEL boyama), insan beyni dokusunda apoptoz belirteci olarak kullanılmıştır. Ancak, TUNEL nekrotik hücreleri de etiketleyebilmektedir. Bu nedenle, farklı hücre ölümü modlarını izlemek için doğru kriterlerin kullanılması zorunludur. Genellikle hücre ölümü tipinin birden fazla karakteristik özelliği dikkate alınmalıdır. Otofajinin tanımlanması için kriterler yakın zamanda yayınlanmış olmasına ve farklı nörodejeneratif hastalıklarda otofajinin belirteçleri tanımlanmış olmasına rağmen, bunların ACD oluşumunun göstergesi olduğundan emin olmak henüz mümkün değildir.
Nörodejeneratif hastalıklarda hücre ölüm mekanizmalarına ilişkin çok sayıda kanıt, in vitro hücre kültür sistemleri veya in vivo modellerden gelmektedir. Bu modeller, akut toksine maruz kalma veya hastalıkta bulunan genetik mutasyonlar kullanmaktadır, nörodejeneratif hastalıklarda apoptoz ve diğer hücre ölümü formlarının nöronal hücre ölümünde önemli roller oynadığı görüşüne katkıda bulunmaktadır. Bununla birlikte modeller, sadece bir toksinin veya bir genin hücre ölümü üzerindeki etkisini inceleme eğiliminde olduklarından sınırlıdır ve genellikle hastalarda gözlenen uzun süreli dejenerasyonla ilgili olmayabilecek hakaretlere akut maruz kalmayı içermektedirler. Bununla birlikte, nörodejeneratif hastalıklarda nöronal hücre ölümünün biyokimyasal mekanizmaları hakkındaki bilgileri büyük ölçüde arttırmaktadırlar.
Alzheimer Hastalığı
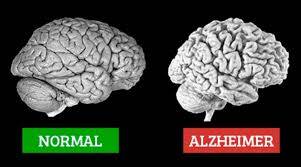 AD en sık görülen nörodejeneratif hastalıktır. Klinik olarak ilerleyici hafıza kaybı ve bilişsel disfonksiyon ile karakterize edilmektedir ve ciddi demansa neden olmaktadır. AD patolojisi, hipokamp-pal bölgelerinden orta ve büyük piramidal nöronların kaybını, amiloid filamanları ve hiperfosforile taudan oluşan hücre içi nörofibriler düğümleri içeren hücre dışı plakların varlığını içermektedir. Ailesel AD, amiloid öncü proteini veya presenilin-1 veya -2’deki mutasyonlardan kaynaklanmaktadır. Presenilinler, 7-sekretaz aktivitesinde, amiloid öncü proteininin proteolitik işlenmesinden sorumlu olan amiloid peptidi üreten önemli bir rol oynamaktadır. AD mutasyonları, oligomerizasyona eğilimli, fibriller ve plaklar oluşturan, biraz daha büyük bir peptit olan p-amiloid-42’nin artan üretiminin eşlik ettiği değiştirilmiş işlemeye yol açmaktadır ve AD’de nöronal hücre ölümüne neyin yol açtığı belirsizdir.
AD en sık görülen nörodejeneratif hastalıktır. Klinik olarak ilerleyici hafıza kaybı ve bilişsel disfonksiyon ile karakterize edilmektedir ve ciddi demansa neden olmaktadır. AD patolojisi, hipokamp-pal bölgelerinden orta ve büyük piramidal nöronların kaybını, amiloid filamanları ve hiperfosforile taudan oluşan hücre içi nörofibriler düğümleri içeren hücre dışı plakların varlığını içermektedir. Ailesel AD, amiloid öncü proteini veya presenilin-1 veya -2’deki mutasyonlardan kaynaklanmaktadır. Presenilinler, 7-sekretaz aktivitesinde, amiloid öncü proteininin proteolitik işlenmesinden sorumlu olan amiloid peptidi üreten önemli bir rol oynamaktadır. AD mutasyonları, oligomerizasyona eğilimli, fibriller ve plaklar oluşturan, biraz daha büyük bir peptit olan p-amiloid-42’nin artan üretiminin eşlik ettiği değiştirilmiş işlemeye yol açmaktadır ve AD’de nöronal hücre ölümüne neyin yol açtığı belirsizdir.
Bununla birlikte, AD olgularında apoptotik morfoloji bildirmeyen başkaları bunu tartışmıştır ve İn vitro modeller, p-amiloidin apoptozu indükleyebileceğini göstermektedir. Presenilin mutasyonları nöronları apoptoz indüksiyonuna ve eksitotoksisiteye duyarlı hale getirmektedir. Aslında amiloid birikiminin AD’de eksitotoksisiteye duyarlılığın artmasına neden olduğu ileri sürülmüştür ve NMDA reseptörlerinin aşırı aktivasyonu, bir sıçan modelinde amiloid kaynaklı dejenerasyona spesifik olarak bağlanmıştır. Ayrıca, eksitotoksisitenin AD’nin sonraki evrelerinde daha önemli bir rolü olabileceği öne sürülmüştür. Otofaji AD modellerine bağlı olmasına rağmen, bunun bir hücre ölüm yolunun bir parçası olduğuna dair kanıt yoktur.
Parkinson Hastalığı
PD, özellikle 55 yaş üstü insanları etkileyen ikinci en yaygın nörodejeneratif hastalıktır. Patolojik olarak, substantia nigra pars compacta’daki dopaminerjik nöronların dejenerasyonu ve hayatta kalan nöronlar içinde eozinofilik intrasitoplazmik inklüzyonların (Lewy cisimcikleri) varlığı ile karakterizedir. Bu, bradikinezinin, istirahat titremesinin ve sertliğinin klinik özelliklerinin doğrudan nedeni olan striatumda dopamin tükenmesine yol açmaktadır. Substantia nigra içinde dopaminerjik nöronların yaklaşık % 50-60’ında bir kayıp olduğunda PD’nin klinik semptomları belirginleşmektedir. Bu nedenle PD, nöronal hücre kaybının gözlemlenen klinik özellikler için doğrudan sorumlu olduğu bir nöro-dejeneratif hastalığa iyi bir örnektir. PD’nin nedeni büyük olasılıkla genetik yatkınlıkla çok faktörlüdür, çevresel toksinler ve yaşlanma hem kalıtsal hem de sporadik PD için hastalığın başlaması ve ilerlemesinde önemli faktörlerdir. Bugüne kadar, en az 13 PARK genindeki mutasyonlar, ailesel PD’nin patogeneziyle ilişkilendirilmiştir. Bunlar, sinu-klein, parkin, PTEN ile indüklenen kinaz 1 (PINK1), DJ-1, lösin açısından zengin tekrar kinaz2 (LRRK2) ve ubikuitin karboksi terminal hidrolaz L1 (UCHL1) proteinlerini kodlayan genlerdeki mutasyonları içermektedir. Bunlardan parkin ve UCHL1, hasarlı veya yanlış katlanmış proteinleri parçalayan ubikitin-proteazom sistemine (UPS) bağlıdır. Ayrıca, parkin, PINK1, DJ-1 ve Omi / Htra2 dâhil olmak üzere bu genlerin bir kısmı mitokondri ile bağlantılıdır, mitokondriyal fonksiyonda ve oksidatif strese dirençte rol oynayabilmektedir. PD’de dopaminerjik nöron kaybını başlatan moleküler mekanizmalar bilinmemektedir.
Substansi nigra PD post mortem dokusunda nöromelanin içeren hücrelerde TUNEL boyaması ile birlikte apoptotik kromatin kümelerinin varlığı, apoptotik hücre ölümünün PD’de nöron kaybına katkıda bulunduğunu düşündürmektedir ve ancak, diğerleri bu bulguları doğrulayamamıştır. Bu hücrelerde aktive edilmiş kaspaz-3 de gözlenmiştir. PD beyninin postmortem çalışmalarında ekstrinsik apoptotik yolun rolüne ilişkin kanıtlar da vardır. Bunlar PD hastalarının orta beyinindeki TNFa, çözünür Fas ve Fas adaptör protein FADD düzeylerinin artmasıyla ilişkilidir. Önemli olarak PD beyinlerinde nöromelanin içeren substantia nigra nöronlarında artmış aktif kaspaz-8 saptanmıştır.
 Mutant a-sinükleinin indüklenebilir ekspresyonu proteazom aktivitesini azaltmaktadır ve mitokondriya bağlı apoptoza duyarlılığı arttırmaktadır. Nigrostriatal sistemde hedeflenen a-sinükleinin aşırı ekspresyonu yeni bir PD hayvan modeli sağlamıştır. Bu modelde nigral dopamin nöronlarının kaspaz-9 aktivasyonu ile seçici dejenerasyonu vardır. Bazı erken çalışmalar, daha sonraki araştırmalar bu hipotezi desteklemese de, PH’da eksitotoksisite için bir rol önermiştir ve bununla birlikte, PD’de ACD için bir rol olabilmektedir. Ultrastrüktürel muayenede PD hastalarında substantia nigra’nın melanize nöronlarında otofagosom benzeri yapılar saptanmıştır. Substantia nigra’nın katekolaminerjik nöronlarındaki nöromelanin granüllerinin çift zar tarafından sınırlandığı ve aslında hücreyi sitozolde öldürücü birikiminden korumak için dopamin ve metabolitleri sekeste eden otofagosomlar olabileceği bildirilmiştir. Bu bulguları desteklemek için dopamin ve MPP + ‘nın insan nöroblastom hücrelerinde ACD indüklediği gösterilmiştir.
Mutant a-sinükleinin indüklenebilir ekspresyonu proteazom aktivitesini azaltmaktadır ve mitokondriya bağlı apoptoza duyarlılığı arttırmaktadır. Nigrostriatal sistemde hedeflenen a-sinükleinin aşırı ekspresyonu yeni bir PD hayvan modeli sağlamıştır. Bu modelde nigral dopamin nöronlarının kaspaz-9 aktivasyonu ile seçici dejenerasyonu vardır. Bazı erken çalışmalar, daha sonraki araştırmalar bu hipotezi desteklemese de, PH’da eksitotoksisite için bir rol önermiştir ve bununla birlikte, PD’de ACD için bir rol olabilmektedir. Ultrastrüktürel muayenede PD hastalarında substantia nigra’nın melanize nöronlarında otofagosom benzeri yapılar saptanmıştır. Substantia nigra’nın katekolaminerjik nöronlarındaki nöromelanin granüllerinin çift zar tarafından sınırlandığı ve aslında hücreyi sitozolde öldürücü birikiminden korumak için dopamin ve metabolitleri sekeste eden otofagosomlar olabileceği bildirilmiştir. Bu bulguları desteklemek için dopamin ve MPP + ‘nın insan nöroblastom hücrelerinde ACD indüklediği gösterilmiştir.
Huntington Hastalığı
HD, bir dizi trinükleotid tekrar bozukluğundan biridir ve Huntingtin proteininin N-ucunda çevrilmiş bir CAG tekrarının baskın kalıtsal olarak genişlemesinden kaynaklanmaktadır. CAG genişlemesinin uzunluğu, hastalık semptomlarının başlangıç yaşı ile ters orantılıdır. Ana klinik semptom, neostriatumdaki orta dikenli nöronların seçici kaybının bir sonucu olan genelleştirilmiş istemsiz hareketlerin ortaya çıkmasıdır. Hastalık patolojisi, mutant avcılık içeren nükleer kapanımların varlığı ile karakterizedir. HD’de nöronal hücre ölümü toksik mutasyona uğramış avcılık fragmanlarının birikimi ile bağlantılı olabilmektedir, çünkü avcılık CAG tekrarının 35’in üzerine yayılması nöronal hücre ölümüyle sonuçlanmaktadır. Bir dizi etkileşen protein tanımlanmış olmasına rağmen, avlanmanın fizyolojik rolü bilinmemektedir.
Kaspazların HD beyinlerinde aktive olduğu gösterilmiştir. İlginç bir şekilde, kendisinin avlanması kaspazlar için bir substrat olup, toksik olabilen poliglütamin kanalını içeren kesilmiş fragmanlar üretmektedir. Eksitotoksisitenin HD patogenezinde rol oynadığı ileri sürülmüştür. HD’de kaybolan orta dikenli nöronlar, korteksten glutamat salınan nöronlar tarafından innerve edilmektedir ve glutamat reseptör agonistlerinin sıçan striatumuna uygulanması üzerine seçici olarak dejenere olmaktadır. Erken evre HD hasta beyinlerinin ölüm sonrası analizi, NMDA reseptör agonisti, kinolinik asit ve öncüsü 3-hidroksi-kynurenin seviyelerinin arttığını göstermektedir, bu da HD’de endojen bir eksitotoksin olarak işlev gösterebileceğini düşündürmektedir. Ayrıca mutant avustinin ekspresyonu, glutamat alımının azalması, değişen insan ticareti ve glutamat reseptörlerinin işlevselliği dahil glutamat nörotransmisyonundaki değişikliklerle ilgilidir. 
Her ne kadar avcılıkta farklı mutasyonlar ifade eden transgenik farelerden dikenli kültürlenmiş ortam eksitotoksik hasara karşı daha duyarlı olsa da, in vivo deneyler çelişkili sonuçlar vermiştir. Bununla birlikte, HD hastalarında mutant avcılık ekspresyonu ile eksitotoksisite arasında doğrudan bir bağlantı gösterilmemiştir. Otofaji, avcılık yoluyla uyarılmaktadır, ancak bunun ACD ile ilişkili olup olmadığı bilinmemektedir. Paradoksal olarak, bazı mutant avcılık formları nöronları hücre ölümüne karşı koruyabilmektedir.
İskemi
İskemi veya inme, beyindeki oksijen, glikoz ve trofik desteğin lokal olarak yok olmasına yol açan kan dolaşımındaki bir kesintinin neden olduğu akut bir durumdur. Nöronlar ATP üretmek için sürekli bir oksijen ve glikoz kaynağına bağımlı olduğundan, iskemi sırasında ATP kaybı iyon gradyanlarının hızlı bir şekilde dağılmasına neden olarak su ve hücre şişmesi, lizis ve hücre ölümüne yol açmaktadır.
İskemi, ilk nöbetten günler sonra ortaya çıkan akut nöronal hücre ölümü ve gecikmiş ölüm ile karakterizedir. Hücre ölümünün ilk aşaması nekrotik ve gecikmiş ölüm apoptotiktir. İskemik çekirdekteki nöronal hücre ölümü nekrotik olma eğilimindedir, penumbra bölgesinde ise apoptotiktir, bu da hakaretin şiddetinin hücre ölümü modunu belirlediğini düşündürmektedir. Hücre ölümünün her iki fazı da NMDA reseptörlerinin antagonizması ile bloke edilebilmektedir. Bu hücre ölümü eksitotoksiktir, bu nedenle nekroz ve apoptozun indüklenmesi açısından aynı özellikleri paylaşmaktadır. Beclin 1’in yukarı regülasyonu, iskemik penumbrada, otofaji markeri LC3’ün iskemik nöronlardaki vakuolik yapılara hücre altı yeniden dağılımı ile birlikte iskemi sırasında otofajinin indüklendiğini göstermektedir. Ancak ACD kesin olarak gösterilmemiştir.
Kaynakça:
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6213751/
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4514105/
https://www.nature.com/articles/cddis2017286
Yazar: Özlem Güvenç Ağaoğlu
