Oligodendrositlerin ve Schwann hücrelerinin temel işlevi miyelin oluşumudur. Miyelin, aksonal segmentlerin izolatörü olarak işlev görür ve 200 m/saniyeye kadar olan yüksek sinir iletim hızı için ön koşuldur. Glial hücrelerin aksonlarla ilişkisi omurgasızlarda da bulunur. Omurgalıların Remak hücrelerine benzer akson yutkunmakta olan hücreler, çoğu omurgasızda bulunur. Miyelinin oligodendrositler ve Schwann hücreleri tarafından oluşumu filogenetik olarak yaklaşık 400 milyon yıl önce omurgalıların bir buluşudur diyebiliriz. Çenesiz balık dışındaki tüm omurgalılar (domuz balığı ve lamprey’ler) oligodendrositlere sahiptir. Miyelinin evrimde ortaya çıkışı, omurgalıların ve özellikle de sinir sistemlerinin gelişimini hızlandırdı. Sinirbilimcilerin çoğu bile oligodendrositlerin omurgalıların evrimi için önemini takdir etmez. Beynin evrimsel gelişimi ile nöron sayısının insanda 100 milyara kadar yükseldiği genel bilgi gibi görünmekle birlikte, tüm bu nöronların ancak miyelin yüzünden karmaşık bir şekilde birbirine bağlanabileceği çok açık değildir. Bu, aşağıdaki örnek ile kolayca gösterilebilir. Sinir iletim hızını arttırmak için bir strateji miyelin oluşturmak, diğeri ise akson çapını arttırmaktır.
Kalamar’ın içindeki dev aksonlar, 1 mm’ye kadar çapa sahiptir ve miyelinli motor aksonlarınki ile karşılaştırılabilir iletim hızlarına ulaşır. İnsan optik siniri, yüksek hızda hareket eden yaklaşık 1 milyon miyelinli aksona sahiptir. 1 mm’lik çapı 1 mm olan kalamar devi akson versiyonu, 0.75 m’lik bir akson çapına eşittir.
Oligodendrositlerin Morfolojisi
Tüm beyaz madde izleri miyelin oluşturmak için oligodendrositler içerir. Oligodendrositler, ayrıca gri maddede de bulunur. Oligodendrositler, merkezi sinir sisteminin miyelini oluşturan hücreler olarak çok iyi bilinirken, doğrudan miyelin kılıfına bağlı olmayan oligodendrositler de 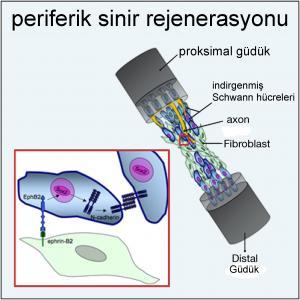 vardır. Bu uydu oligodendrositleri tercihen gri maddede bulunur ve şimdiye kadar astrositlere benzer şekilde iyonik homeostazı düzenlemeye yarayan bilinmeyen fonksiyonlara sahiptir. Sadece sıçan, fare ve insanın retinası, miyelinleştirici oligodendrositlerden yoksundur, tavşan ve civciv retinasının her ikisi de kısmen miyelinlidir. Miyelin oluşturan oligodendrositler, bir miyelin segmentine bağlanan birkaç işleme (40’a kadar) sahiptir. Bu bölümlerin her biri birkaç yüz mikrometre uzunluğundadır ve ayrıca internod olarak da adlandırılır. Segmentler, 1 mikrondan daha az bir alana yayılan Ranvier düğümü olarak bilinen yapılar tarafından kesilir. Düğümde, iç bölgeler ile karşılaştırıldığında, akson miyelin tarafından sarılmaz. İntermodal parçanın sonu daha fazla sitoplazma içerir ve akson ile septat benzeri kavşaklar oluşturan paranodal halka olarak adlandırılan formlar oluşturur. Ek olarak, astrosit işlemleri nodal bölgedeki aksonal zar ile temas eder.
vardır. Bu uydu oligodendrositleri tercihen gri maddede bulunur ve şimdiye kadar astrositlere benzer şekilde iyonik homeostazı düzenlemeye yarayan bilinmeyen fonksiyonlara sahiptir. Sadece sıçan, fare ve insanın retinası, miyelinleştirici oligodendrositlerden yoksundur, tavşan ve civciv retinasının her ikisi de kısmen miyelinlidir. Miyelin oluşturan oligodendrositler, bir miyelin segmentine bağlanan birkaç işleme (40’a kadar) sahiptir. Bu bölümlerin her biri birkaç yüz mikrometre uzunluğundadır ve ayrıca internod olarak da adlandırılır. Segmentler, 1 mikrondan daha az bir alana yayılan Ranvier düğümü olarak bilinen yapılar tarafından kesilir. Düğümde, iç bölgeler ile karşılaştırıldığında, akson miyelin tarafından sarılmaz. İntermodal parçanın sonu daha fazla sitoplazma içerir ve akson ile septat benzeri kavşaklar oluşturan paranodal halka olarak adlandırılan formlar oluşturur. Ek olarak, astrosit işlemleri nodal bölgedeki aksonal zar ile temas eder.
Astrositler gibi oligodendrositler de konneksinlerin oluşturduğu boşluklarla birbirine bağlanır. Astrositlere kıyasla oligodendrositler için belirgin konneksin proteinleri vardır. Connexin proteinlerindeki mutasyonlar hipomiyelinizasyona ve lökodistrofiler gibi insan patolojilerine yol açar.
Oligodendrositlerin gelişimi
Miyelin oluşumu kemirgenlerde yaklaşık doğumda başlar ve doğumdan 2 ay sonra tamamlanır. İnsanlarda fetal yaşamın ikinci yarısında başlar ve omurilikte gelişir. Zirve aktivitesi doğum sonrası ilk yıldan 20 yaşına kadar devam eder. Genellikle daha büyük aksonların daha kalın miyelin oluşturduğu belirtilmektedir. Gelişme sırasında oligodendrositler, serebrum için lateral ventriküllerin subventriküler bölgesi veya serebellum için dördüncü ventrikül gibi subventriküler bölgede bulunan öncülerden ortaya çıkar. Omurilikte oligodendrositler, nöral tüpün ventral bölgelerinden kaynaklanır ve optik sinirde, üçüncü ventrikülden sinire göç ederler. Hedeflerine göç eden oligodendrosit öncü hücreleridir ve daha olgun oligodendrositlere farklılaşırlar. Oligodendrosit progenitör hücrelerinin çoğalması, ağırlıklı olarak nöronlardan değil, trombosit kaynaklı büyüme faktörü (PDGF) veya fibroblast büyüme faktörü (FGF) gibi astrositlerden salınan bir dizi büyüme faktörü ile kontrol edilir. Dahası, içsel bir saat sadece hücre bölünmesini saymaz, aynı zamanda zamanı da algılar. Böylece, içsel mekanizmalar ve çevre, miyelinasyon için gereken uygun miktarda oligodendrositleri kontrol eder. Aşırı miktarda üretilen (normal koşullar altında ortaya çıkan) oligodendrositler apoptoz ile elimine edilir. Oligodendrosit progenitör hücrelerinin çoğalması, ağırlıklı olarak nöronlardan değil, trombosit kaynaklı büyüme faktörü (PDGF) veya fibroblast büyüme faktörü (FGF) gibi astrositlerden salınan bir dizi büyüme faktörü ile kontrol edilir. Dahası, içsel bir saat sadece hücre bölünmesini saymaz, aynı zamanda zamanı da algılar. Böylece, içsel mekanizmalar ve çevre, miyelinasyon için gereken uygun miktarda oligodendrositleri kontrol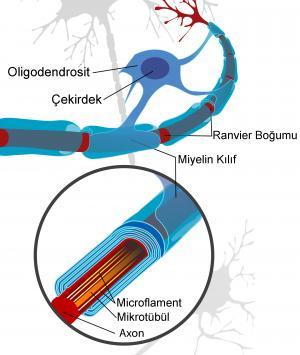 eder. Aşırı miktarda üretilen (normal koşullar altında ortaya çıkan) oligodendrositler apoptoz ile elimine edilir. Oligodendrosit progenitör hücrelerinin çoğalması, ağırlıklı olarak nöronlardan değil, trombosit kaynaklı büyüme faktörü (PDGF) veya fibroblast büyüme faktörü (FGF) gibi astrositlerden salınan bir dizi büyüme faktörü ile kontrol edilir. Dahası, içsel bir saat sadece hücre bölünmesini saymaz, aynı zamanda zamanı da algılar. Böylece, içsel mekanizmalar ve çevre, miyelinasyon için gereken uygun miktarda oligodendrositleri kontrol eder. Aşırı miktarda üretilen (normal koşullar altında ortaya çıkan) oligodendrositler apoptoz ile elimine edilir.
eder. Aşırı miktarda üretilen (normal koşullar altında ortaya çıkan) oligodendrositler apoptoz ile elimine edilir. Oligodendrosit progenitör hücrelerinin çoğalması, ağırlıklı olarak nöronlardan değil, trombosit kaynaklı büyüme faktörü (PDGF) veya fibroblast büyüme faktörü (FGF) gibi astrositlerden salınan bir dizi büyüme faktörü ile kontrol edilir. Dahası, içsel bir saat sadece hücre bölünmesini saymaz, aynı zamanda zamanı da algılar. Böylece, içsel mekanizmalar ve çevre, miyelinasyon için gereken uygun miktarda oligodendrositleri kontrol eder. Aşırı miktarda üretilen (normal koşullar altında ortaya çıkan) oligodendrositler apoptoz ile elimine edilir.
Hala astrositlere ve oligodendrositlere neden olabilen oligodendrosit progenitör hücreleri, sadece gelişim sırasında bulunmaz, aynı zamanda yetişkin oligodendrosit öncü hücreleri olarak adlandırılan olgun beyinde de bulunur. Multipl skleroz gibi demiyelinizan hastalıklarda remiyelinizasyon kaynağı olarak kabul edilirler. Transkripsiyon faktörü Olig-2 veya proteoglisan NG2 gibi bu öncü hücrelerin tanımlanmasına yardımcı olan birkaç farklı belirteç vardır. Bu NG2 pozitif hücreler son zamanlarda önemli bir ilgi görmüştür. Astrositler ve oligodendrositler halinde gelişme kapasitelerine sahip olsalar da, ana yol oligodendrosit soyları ile sınırlı gibi görünmektedir. Bu yetişkin öncü hücrelerinin aksonlarla etkileşime girdiği görülmektedir. Glutamat reseptörleri eksprese eder ve aksonun aktivitesini algılarlar, bu, aktiviteye bağlı bir şekilde glutamat salmaktadır. Bu, aksonların oligodendrosit progenitör hücrelerinin farklılaşmasını nasıl kontrol edebileceği için potansiyel bir mekanizma gibi görünmektedir.
Schwann hücreleri
Schwann hücreleri, periferik sinir sistemindeki oligodendrositlerin hücresel karşılığıdır. Oligodendrositlere benzer şekilde miyelin kılıfını oluştururlar. Oligodendrositin aksine, her Schwann hücresi sadece bir aksonal segment ile ilişkilidir. Oligodendrositler ve Schwann hücrelerinin oluşturduğu miyelin yapısı benzer bir yapıya sahipken, aynı protein grubundan oluşmaz. Santral ve periferik miyelin bazik protein miyelini paylaşırken, periferik sinir sistemi miyelinle ilişkili glikoprotein veya proteolipid proteininden yoksundur, ancak protein P0 ve PMP22’yi eksprese eder. Gelişme sırasında, Schwann hücreleri farklılaşmamış göç eden nöral kret hücrelerinden türetilir. Olgunlaşmamış Schwann hücreleri, miyelinleştirici veya miyelinleştirici olmayan Schwann hücreleri üretir. İkincisi, miyelini oluşturmadan birkaç aksonu gevşekçe içine alır.
Duyusal sempatik ve parasempatik ganglionlardaki nöronal hücre gövdeleri, uydu hücreleri olarak bilinen düzleştirilmiş kılıf benzeri hücreler ile çevrilidir. Nöromüsküler bir kavşakta bulunan akson terminalleri ayrıca terminal glia gibi özel glial hücreler tarafından kaplanır.
Miyelin Kılıfları
Miyelin kılıfı, aksonun oligodendrosit veya schwann hücre işlemleriyle sarılmasıyla oluşturulur. Hücre içi bölme, sadece 30 angströme yayılan çok fazla sıkıştırılmıştır ve elektron mikroskobunda ana yoğun çizgi olarak adlandırılan tek bir çizgi olarak görünür. Lipit iki tabakasının dış yüzeyi, hücre dışı boşlukla ayrılmış ayrı bir çizgi olarak görünür. Bu nedenle, bu çift intraperdiod çizgisi olarak tanımlanır. Bu yoğun sıkıştırma nedeniyle miyelin tamamen hidratlanır ve kuru kütlesi yaklaşık % 70 lipit ve % 30 protein içerir. Sadece miyelinde bulunan ve bu yapının oluşumu için gerekli olan çok sayıda spesifik protein vardır. Santral sinir sistemi miyelininin ana proteinleri miyelinle ilişkili glikoprotein (MAG), miyelin temel proteini (MBP), miyelin oligodendrosit glikoproteinidir (MOG), proteolipidprotein (PLP)/DM20 ve PMP22. Bu proteinler sadece miyelin oluşturan hücreler, yani merkezi sinir sistemindeki oligodendrositler veya periferik sinir sistemindeki Schwann hücreleri tarafından üretilir ve böylece miyelin hücreleri için mükemmel belirteçler olarak işlev görür. Miyelin katmanlarının içinde, schmidt-lantermann insizlikleri adlı bir sitoplazmik aralık içeren bir tür yol vardır. Bunlar miyelin için trofik destek sağlar.
Omurgalı aksonların hepsi miyelinli değildir, ancak genel olarak 1 mikrondan büyük olan aksonlar miyelinlidir. Son çalışmalar, aksonların miyelin kılıfının kalınlığını belirleyen oligodendrosit için bir sinyal sağladığını göstermektedir. Akson tarafından sağlanan bir önemli sinyalleşme mekanizması, oligodendrositler tarafından ifade edilen ErbB reseptör tirozin kinazlarına bağlanan büyüme faktörü neuregulin-1’dir. Schwann hücrelerinde de benzer bir sinyal mekanizması mevcuttur. Bu etkileşim aksonal çap ile aksonal çap artı miyelin kılıfı arasında tanımlanmış bir orana yol açar; bu oran genellikle 0.6 ile 0.7 arasındadır.
Miyelin hücrelerinin aksonlara metabolik destek sağladığı uzun zamandır öne sürülmektedir. Piruvat veya laktat gibi glia kaynaklı glikolitik ürünlerin serbest bırakıldığı ve akson tarafından alındığı tahmin edilebilir. Bu, periferik sinir sistemi için daha da önemli olabilir, çünkü somadaki metabolitlerin büyük hayvanlarda bir metreden daha uzun mesafeler için taşınması gerekir.
Miyelin Saltatory Sinir İletimini Sağlar
Ranvier düğümü, saltatory iletim (“atlamak” anlamına gelen Latince “saltare” kelimesinden) kelimesine izin veren, yani yalnızca düğümdeki eylem potansiyellerinin üretilmesini sağlayan yüksek yoğunluklu bir sodyum kanalı içerir. Böylece, aksiyon potansiyeli sadece düğümde tetiklenir, daha sonra pasif olarak yayılır ve böylece hızlı bir şekilde bir sonraki aksiyon potansiyelinin üretildiği bir sonraki düğüme geçer. Böylece eylem potansiyeli düğümden düğüme atlar. Bu sadece daha hızlı değildir, fakat daha az enerji harcar, çünkü sodyum iyonları yalnızca düğümde birikir ve Na+/K+’nın aktivitesinden dolayı hücre dışı boşluğa geri taşınması gerekir. Miyelin oluşumundan önce sodyum kanalları akson uzunluğu boyunca rastgele dağılır. Bununla birlikte glial örtme sırasında, sodyum kanalları sahada daha sonra ranvier düğümü haline gelen gevşek kümeler oluşturmaya başlar. Daha sonra, kompakt miyelin oluşumundan sonra, sodyum kanalları miyelin kılıfının altındaki zardan ve sadece düğümdeki kümeden kaybolur. Bu kümeleme, miyelinleştirici hücre zarı ile glonmedin, nörofasin ve NCAM gibi hücre adezyon moleküllerini içeren aksonal membran arasındaki protein etkileşimleri ile desteklenir. K+ kanalları nodal bölgede daha az sıkıca konsantredir.
Miyelin Hücreleri ve Hastalıkları
Oligodendrositleri içeren en sık görülen hastalık multipl sklerozdur. Beyin ve omuriliğin tanımlanmış alanlarında miyelin kaybı nedeniyle aksonal iletkenliğin bozulmasına neden olur. Yeniden miyelinasyon nedeniyle iyileşme olabilir, ancak sıklıkla sürekli nörodejenerasyona yol açan tekrarlamalar ortaya çıkar. Oligodendrositlerin kaybının birincil nedeni henüz bilinmemektedir. Demiyeline edilmiş bölgenin, infiltre lenfositler ve makrofajlar ve aktive edilmiş mikroglia gibi enflamatuar hücreler içerdiği açıktır. Bu hücreler hasar zincirini kuvvetlendirebilir veya hatta başlatabilir. Santral sinir sisteminin kalıtsal diğer miyelin hastalıkları pelizaeus-merzbacher hastalığı ve pelizaeus-merzbacher benzeri hastalıklar ve diğer lökodistrofi formlarıdır. Genetik olarak belirlenmiş patolojilerin çoğu, miyelin proteinleri veya konneksinlerdeki mutasyonlarla ilişkilidir, moleküler varlıklar boşluk kavşakları oluşturur. Schwann hücresi miyelindeki merkezi veya merkezi sinir sistemi mutasyonlarına benzer veya aralıklı kavşak proteinleri charcot-marie-tooth hastalığı gibi nöropatilere yol açar. Bu, periferik miyelin oluşumunun omurgalıların hayatta kalması için de gerekli olduğunu açıkça ortaya koymaktadır.
Kaynakça:
Britannica
Yazar: Tuncay Bayraktar
