Apoptozun (programlı hücre ölümü), birçok farklı tetikleyicisi vardır. Bütün bu tetikleyiciler, kaspaz adı verilen parçalayıcı proteinleri aktifleştirir. Hücre içerisindeki yüzlerce farklı proteini, genomu, organelleri ve hücre iskeletini parçalamak; hücrenin küçülmesine, parçalara ayrılmasına ve ölmesine yol açar.
Genel dogma, apoptozun geri dönüşümü olmadığı yönündedir. Hong kong Üniversitesi’nde araştırmacı olan Tang ise bunun gerçekten böyle olup olmadığını araştırdı. Yaptığı çalışmada, çok sayıda kanser hücresini etanol gibi toksinlere maruz bıraktı ve kaspaz aktivasyonu ve hücre küçülmesi gibi apoptoz belirtileri ortaya çıkana kadar bekledi. Sonraki aşamada, deneyin sonunda ölü hücreleri atmak yerine onları yıkadı ve taze besiyeriyle gece boyunca bekletti.
Hücreler sabah tekrar kontrol edildiğinde ilginç şekilde bazı hücreler normal morfolojilerini (şekillerini) geri kazandı. Bu olay anastasis olarak adlandırıldı. Apoptoz Yunancada düşüş anlamına gelir ve bu süreç hücrelerin doğal geri dönüşümünü kolaylaştırır. Diğer taraftan anastasis ise yükseliş anlamına gelir. Bilim insanları başlangıçta hücrelerin ölümden dönebileceği konusunda şüpheciydi. Bu nedenle bu konuda yapılan yayınlar, son üç yılda 11 defadan fazla reddedildi. Bu nedenle John Hopkins Üniversitesi’ne geçen Tang, bu konuda daha fazla araştırma yapmaya devam etti. Burada insan kanser hücrelerinin yanı sıra fare karaciğeri, sıçan kalbi, dağ gelinciği beyni ve insan fibroblast (deri) hücreleri üzerinde de çalışmalar yaptı. Hücreler, DNA hasarı ve hücre parçalanmasından etkilense de, apoptozun ileri bir evresinin ardından yenilenebiliyordu.
2012’de anastasis resmi olarak adlandırıldığından beri araştırmacılar, hücrelerin apoptoz tarafından ciddi şekilde hasar gördükten sonra bile 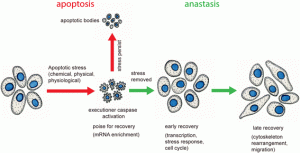 nasıl yenilenebildiğini araştırmaya devam ettiler. Bilim insanları insan hücrelerinde, parçalanmış mitokondrinin (hücrede enerji üretimini sağlayan organel) tekrar bütün haline geldiğini ve hücrelerin hayata dönebilmesi için apoptoz sırasında bir grup mRNA’nın üretilip saklandığını gözlemlediler. Ayrıca anastasisin varlığına dair kanıtlar drosophilada (meyve sineği) da gözlemlendi.
nasıl yenilenebildiğini araştırmaya devam ettiler. Bilim insanları insan hücrelerinde, parçalanmış mitokondrinin (hücrede enerji üretimini sağlayan organel) tekrar bütün haline geldiğini ve hücrelerin hayata dönebilmesi için apoptoz sırasında bir grup mRNA’nın üretilip saklandığını gözlemlediler. Ayrıca anastasisin varlığına dair kanıtlar drosophilada (meyve sineği) da gözlemlendi.
Hücreler Nasıl Hayatta Kalır?
Hücreler; günlerce, aylarca ve hatta yıllarca yaşayabilir. Fakat apoptoz başladığında, hücre hızlı bir şekilde ölüme gider. Kaspazların aktivasyonundan sonra 10 dakika içerisinde hücre, gözle görülür şekilde değişime uğrar. Bu süreç sırasında hücre küçülür ve DNA parçalara ayrılır. Ayrıca kaspazın hücre zarı ile etkileşime geçmesi sonucu oluşan fosfotidilserin molekülü, fagositik hücreler (başka hücreleri sindiren bağışıklık sistemi hücreleri) için de sinyal oluşturur.
Apoptoz, çok sayıda farklı yolla tetiklenir ve bu yollar; hücrenin DNA’sını, organellerini ve hücre iskeletini parçalayan kaspaz isimli enzimleri aktive eder. Kaspazlar ayrıca ölen hücrelerin kalıntılarının sindirilebilmesi için diğer hücrelerin de gelmesini sağlar. Fakat anastasis apoptozun geç evrelerinde meydana gelirse, hayatta kalan hücreler ciddi DNA hasarları taşıyabilir ve diğer genetik hasarlar tümör oluşumuna neden olabilir.
2015 yılında, laboratuvar ortamında çoğaltılan insan hücreleriyle çalışan Ichim Tait ve meslektaşları, başarısız olmuş apoptoz adı verilen anastasisden farklı bir kavram ortaya attılar. Bu kavram, apoptozun neden olduğu radikal değişikliklerden sonra yenilenen hücreleri ifade eder. Mitokondriler, kaspazların potansiyel tetikleyici sitokrom c’yi dışarı sızdırmaya başladığı zaman, hücredeki diğer tüm mitokondrilerde de senkronize şekilde sızmalar olduğuna inanıldı. Fakat araştırmacılar bu durumu kontrol ettiklerinde, hücredeki tüm mitokondrilerden sadece birkaçının sızma gösterdiğini buldular. Bunun sonucunda, az sayıda kaspaz aktive olur ve hücreler hayatta kalır.
Anastasise benzeyen şekilde başarısız olmuş apoptoz, ölümle sonuçlanmayan apoptoz başlangıcını içerir. Fakat bu apoptoz türünde hücre, kısmen apoptoza girer. Başarılı bir apoptozda, olan kaspaz seviyesinden çok daha azı aktive olur ve bu az sayıda enzim hücreyi kısmen parçalar. Buna karşın Tang’ın bulgularına göre, apoptoz tamamen gerçekleştiğinde bile, hücreler onarılabilir.
Araştırmacılar, time-lapse canlı hücre mikroskopisi yöntemi ile, HeLa hücre parçalarının normal hücre morfolojisini oluşturacak şekilde birleştiğini  gösterdi. Apoptozun nasıl başladığı anastasisin meydana gelmesi açısından önemli değildir. Başlatan koşullar düzelirse anastasis; soğuk, protein açlığı ve toksik kimyasallar gibi koşulların neden olduğu hasarlardan hücreyi kurtarabilir. İleri seviyede apoptoz görülen hücrelerde bile, parçalanmış mitokondri birleşebilir ve normal haline geri dönebilir. Yenilenmeden birkaç saat sonra hücreler, zarlarındaki fosfotidilserin molekülünü de ortadan kaldırarak fagositik hücrelerin hedefinden de kurtulur.
gösterdi. Apoptozun nasıl başladığı anastasisin meydana gelmesi açısından önemli değildir. Başlatan koşullar düzelirse anastasis; soğuk, protein açlığı ve toksik kimyasallar gibi koşulların neden olduğu hasarlardan hücreyi kurtarabilir. İleri seviyede apoptoz görülen hücrelerde bile, parçalanmış mitokondri birleşebilir ve normal haline geri dönebilir. Yenilenmeden birkaç saat sonra hücreler, zarlarındaki fosfotidilserin molekülünü de ortadan kaldırarak fagositik hücrelerin hedefinden de kurtulur.
2017 yılında Montell ve Tang birbirlerinden bağımsız şekilde, anastasisin moleküler mekanizmasını yayınladı. Montell’in grubu apoptoza girmiş HeLa hücrelerinde 1,000’den fazla genin aktifleştiğini buldular. Anastasisin moleküler cevabı, otofajiden (hücrede atık yapıların sindirilmesi olayı) sonra hayatta kalan hücrelerin cevabına benzer. Buna ek olarak, apoptozdan önce hücreyi kurtarmak için hücrede biriken mRNA’lar hücreyi anastasise hazırlar. Tang ve arkadaşları; fare karaciğer hücrelerinde; hasarlı mitokondrinin ortadan kaldırılmasıyla, serbest radikallerle ve diğer hücresel bileşenler ilgili genlerin aktivitesinin değiştiğini gözlemlediler.
Apoptozdan Dönüşün Etkileri
Anastasisin bir muhtemel işlevi, geçici bir duruma cevap olarak ortaya çıkan bir hasarın kalıcı olmasını önlemektir. Örneğin, gelişen bir organizmada, rastgele olarak aralıklarla büyüme faktörü eksikliği ortaya çıkabilir ve bu durum hücrelerin hızlıca çoğaldığı gelişim döneminde apoptozu tetikleyebilir. Montell ve arkadaşları, larva beyninde kaspaz aktivasyonu sonrasında hücrelerin hayatta kaldığını ve Drosophila gelişimi sırasında anastasisin görülebildiğini buldu.
Anastasis, evrimsel değişiklikleri de teşvik edebilir. Tang’ın çalışmasında, açlık ve soğuk şoku gibi çevresel stres koşullarının varlığında, Drosophila üreme hücrelerinde anastasisin tekrarlandığı görüldü. Bu durum ise, hücrelerin apoptoz sırasında yeni nesillere geçecek mutasyonları geçirebileceğini gösterir.
Anastasis, basit bir korunmadan daha fazla amaca hizmet edebilir. 2012 yılında Tang ve Montell, apoptozdan kurtulan hücrelerde genetik hasar onarılırken, bazen genomda hataları ortaya çıktığını gözlemledi. Sonuç olarak hayatta kalan hücrelerin bir yüzdesi kromozomal anormalilere sahiptir ve diğer genetik bozukluklar ise tümör gelişimine neden olur. Hücrenin bu şekilde sürekli ölümün kıyısına gelmesi; hasara uğrayan  dokularda (örneğin, sürekli sıcak içeceklerin tüketilmesi sonucu özafagus kanseri ve kronik alkol kullanımı sonucu karaciğer kanserinin ortaya çıkması) yüksek oranda kanser gelişme riskini açıklayabilir. Başarısız olmuş apoptozda bile (iyileşmeden önce hasar daha az ciddiyken) genom bazen stabil olmaz ve hatta bazı hücreler tümör hücrelerine dönüşür.
dokularda (örneğin, sürekli sıcak içeceklerin tüketilmesi sonucu özafagus kanseri ve kronik alkol kullanımı sonucu karaciğer kanserinin ortaya çıkması) yüksek oranda kanser gelişme riskini açıklayabilir. Başarısız olmuş apoptozda bile (iyileşmeden önce hasar daha az ciddiyken) genom bazen stabil olmaz ve hatta bazı hücreler tümör hücrelerine dönüşür.
Hücrenin programlanmış hücre ölümünden dönme yeteneği; bazı kanserlerin tedavi edici yaklaşımlardan kurtulmasında rol oynayabilir. Radyasyon ve yaygın olarak kullanılan kemoterapi ilaçları apoptozu uyarır ve bunlar birçok tümör hücresini öldürürken, hayatta kalan hücreler kanserin nüksetmesine yol açar. Üstelik bu tür terapilerden sağ çıkan kanser hücreleri yeni mutasyonlar geliştirerek, ilaçlara daha fazla dirençli olabilir.
Ayrıca Tang ve meslektaşları, anastasisin Drosophila’da, anjiogenez (damarlanma) ve hücre göçü ile ilgili genleri aktifleştirebildiğini buldu. Anjiogenez de besin emilimini arttırarak ve atıkların uzaklaşmasına yardım ederek hücrelerin apoptozdan kurtulup iyileşmesini sağlar. Ayrıca bu değişiklikler, kanser hücrelerinin yayılımını da arttırır.
Kanser ve anastasis arasındaki potansiyel bağlantının keşfedilmesiyle kanser tedavisi sırasında ve sonrasında ölen bir kanser hücresinde anastasisi baskılamak, kanserin nüksetmesini önlemek için yeni bir tedavi olabilir. Anastasisi hedef almak, kalp kası hücreleri ve nöronlar gibi yenilenemeyen hücrelerin kaybı nedeniyle ortaya çıkan hastalıkların tedavisinde de kullanılabilir. Anastatasisin daha iyi anlaşılması, hücrelerin sadece hastalıktan ve hasardan nasıl kurtulduğu ile ilgili bilgi vermez, aynı zamanda bilim insanların hücre ölümünü daha iyi şekilde anlamasını sağlar.
Kaynakça:
https://www.the-scientist.com/features/cell-death-processes-are-reversible-65338
Yazar: Ayça Olcay
