 Sıcaklık ve ısı birbiriyle ilişkili, ancak farklı kavramlardır. Isı, bir enerji türüdür ve kalorimetre ile ölçülür. Isı, daha sıcak bir maddeden veya nesneden daha soğuk olana doğru akar ve bir enerji transferi oluşur. Enerjinin ısı olarak aktarılması, doğrudan temas yoluyla, kondüksiyonla, radyasyonla, konvektif sirkülasyonda olduğu gibi bir sıvı aracılığıyla ya da bunların çeşitli kombinasyonlarıyla gerçekleşebilir. “İş”in aksine, ısı, maddenin atomlar veya moleküller gibi parçacıklarının stokastik (rastgele) hareketini içerir.
Sıcaklık ve ısı birbiriyle ilişkili, ancak farklı kavramlardır. Isı, bir enerji türüdür ve kalorimetre ile ölçülür. Isı, daha sıcak bir maddeden veya nesneden daha soğuk olana doğru akar ve bir enerji transferi oluşur. Enerjinin ısı olarak aktarılması, doğrudan temas yoluyla, kondüksiyonla, radyasyonla, konvektif sirkülasyonda olduğu gibi bir sıvı aracılığıyla ya da bunların çeşitli kombinasyonlarıyla gerçekleşebilir. “İş”in aksine, ısı, maddenin atomlar veya moleküller gibi parçacıklarının stokastik (rastgele) hareketini içerir.
Isı (iş gibi), iki nesne arasında belli bir süreçle aktarılan bir enerji miktarı olduğu için, her iki nesne de belli bir ısı derecesine sahip değildir. Aksine, bir madde ya da nesne aslında sıcaklık (derece) ve iç enerji gibi özelliklere sahiptir. Belirli bir süreçte ısı olarak aktarılan enerji, her bir nesnenin iç enerjisini eşit ve zıt miktarlarla değiştirir. Isı miktarının işareti aktarımın yönünü gösterir. Örneğin, sistem A’dan sistem B’ye doğru bir aktarımda, negatif işaret, ters yönde akan enerjiyi gösterir.
Uluslararası Birimler Sisteminde (SI), standart ısı birimi, “Calorie” (kalori, Cal) ya da 1925 tarihinden beri “Joule” (jul, J) dür. Isı, etkileşen cisimlerin durumları üzerindeki etkisi ile, örneğin erimiş buz miktarı veya sıcaklık derecesindeki değişim ile ölçülür. Bir maddenin ya da nesnenin, sıcaklık değişimi yoluyla ısısının ölçümü kalorimetri olarak adlandırılır. Kalorimetride, basınç veya hacim gibi sistemin belirli bir seçilmiş durum değişkenine göre “ölçülebilir ısı” tanımlanır. Ölçülebilir ısı, seçilen durum değişkenini değiştirmeden, sistem sıcaklığının değişmesine neden olur. Sabit bir sistem sıcaklığında meydana gelen, ancak durum değişkenini değiştiren ısı transferi, değişkene göre “gizil ısı” olarak adlandırılır. Sonsuz küçük değerlerdeki aktarımlarda, toplam artan ısı transferi, gizil ve ölçülebilir ısıların toplamıdır.
Öz ısı (Özgül Isı, Isınma Isısı)
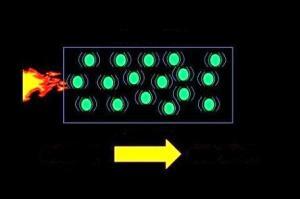 Bir maddenin iç enerjisi arttıkça, parçacıklarının hareketleri de hızlanır. Parçacıklardaki enerji artışı, sıcaklıktaki artışla anlaşılır. Madde ısı kazanır. Bir madde ısı kaybederken de, parçacıklarının hareketleri yavaşlar ve maddenin sıcaklığı da azalır. Öz ısı, özgül ısı ya da ısınma ısısı, bir maddenin ısıyı soğurma (yutma) yeteneğini gösterir ve maddenin 1 gramının sıcaklığını 1°C arttırmak için gereken ısı miktarıdır.
Bir maddenin iç enerjisi arttıkça, parçacıklarının hareketleri de hızlanır. Parçacıklardaki enerji artışı, sıcaklıktaki artışla anlaşılır. Madde ısı kazanır. Bir madde ısı kaybederken de, parçacıklarının hareketleri yavaşlar ve maddenin sıcaklığı da azalır. Öz ısı, özgül ısı ya da ısınma ısısı, bir maddenin ısıyı soğurma (yutma) yeteneğini gösterir ve maddenin 1 gramının sıcaklığını 1°C arttırmak için gereken ısı miktarıdır.
Özgül ısının birimi J / g °C’dir. Suyun özgül ısısı 4,18 J / g °C ya da 1,00 Cal / g °C’tur. Bu, bir gram suyun sıcaklığının bir derece artması için 4,18 jullük ısı enerjisi gerektiği anlamına gelmektedir. Diğer elementlerin öz ısısının sudan daha az olmasının nedeni, suyun hidrojen ve oksijen olmak üzere iki ayrı elementten oluşmasıdır. Maddeler farklı öz ısılara sahiptir. Örneğin, demirin öz ısısı 0,45 J / g °C’dir. Yani, bir gram demirin sıcaklığının bir derece artması 0,45 jullük ısı enerjisi gerektirmektedir. Bakırın öz ısısı 0,37, buzun 2,09, cıvanın 0,12, alkolün 2,54, zeytinyağının öz ısısı ise 1,96 J / g °C’dir. Özetle, öz ısı maddeler için ayırt edici bir özellik anlamını taşımaktadır.
Öz ısının tanımında, maddenin 1 gramının sıcaklığını 1 °C artıran ısı miktarı c (öz ısı) Joule olduğuna göre, hesaplamak için
Isı Miktarı = Kütle x Öz Isı x Sıcaklık Farkı
Q = m . c . Δt bağıntısı kurulur.
Sıcaklık
Bir maddeyi oluşturan atomların ya da moleküllerin hareket (kinetik) enerjilerinin ortalamasına sıcaklık denir. Bir enerji türü olmadığı gibi, maddenin miktarına da bağlı değildir. Termometre ile ölçülür ve birimi °C yani “Celcius”tur. Sıcaklıkları farklı maddelerin arasında, sıcaklık akış yönü (termik akış) sıcaklığı yüksek olandan düşük olana doğru giden bir sıcaklık alışverişi gerçekleşir. Sıcaklık akışı maddelerin sıcaklığı eşitlenene kadar sürer.
Denge Sıcaklığı
Farklı sıcaklıktaki iki madde ya da cisim birbirleriyle temas ettiklerinde, yukarıda söz edildiği gibi bir “ısı alışverişi”nde bulunurlar. Örneğin, haşlanmış sıcak bir yumurta soğuk suyla dolu bir kaba atıldığında, yumurta soğurken su ısınır. Isı enerjisi sıcak yumurtadan soğuk suya akarak suyu ısıtmıştır. Bu ısı alışverişi yumurta ve su aynı sıcaklığa eriştiklerinde yani “denge sıcaklığı”na geldiklerinde durur. Sıcak olanın verdiği ısı enerjisi ile soğuk olanın aldığı ısı enerjisi eşittir. Sıcaklıkları eşit maddeler arasında ısı alışverişi olmaz.
– Bir maddenin, sıcaklıkları farklı, eşit iki miktarı arasındaki denge sıcaklığı, iki miktarın sıcaklıklarının ortalaması alınarak bulunur.
– Bir maddenin, hem sıcaklıkları hem miktarları farklı iki kütlesi arasındaki denge sıcaklığının bulunmasında
(t1 > t2 ise)
Q verilen = Q alınan
m1 . c . Δt = m2 . c . Δt
m1 . (t1 – t denge) = m2 . (t denge – t2) olur.
– Cinsleri, sıcaklıkları ve miktarları birbirinden farklı maddelerin denge sıcaklığının bulunmasında
(t1 > t2 ise)
Q verilen = Q alınan
m1 . c1 . (t1 – t denge) = m2 . c2 . (t denge – t2) olur.
Sıcaklık Değişimi
Herhangi bir madde ısı enerjisi aldığında, atom ve moleküllerinin kinetik enerjisi artar. Dolayısıyla sıcaklığı artmış olur. Eğer madde dışarıya ısı enerjisi veriyorsa kinetik enerjisi azaldığından sıcaklığı azalır. Bir maddedeki sıcaklık değişiminin gerçekleşmesi için gerekli ısı enerjisi, maddenin cinsine (öz ısısına), miktarına (kütlesine) ve ısıtıcının gücüne bağlıdır.
Farklı maddelerin birim kütlelerinde, maddelerin molekül büyüklükleri farklı olduğundan, farklı sayılarda molekül vardır. Molekül büyüklükleri farklı olduğundan, molekül kütleleri de farklıdır ve kinetik enerjilerinin (sıcaklıklarının) değişmesi için gereken ısı enerjisi miktarı da farklı olmaktadır. Aynı miktardaki farklı maddeler eşit sürelerde ısıtıldıklarında, kütlelerindeki molekül sayıları farklı olduğundan ve molekül sayısı az olan (öz ısısı düşük olan) maddenin ortalama kinetik enerjisi daha fazla artacağından, sıcaklığı da daha fazla artacaktır.
Öz ısısı düşük olan maddelerin sıcaklığı hızla yükselirken, öz ısısı büyük olan maddelerin sıcaklığı daha yavaş yükselir. Öz ısısı düşük olan maddeler, öz ısısı büyük olan maddelerden daha çabuk soğurlar. Birinin öz ısısı küçük, diğerinin öz ısısı büyük olan, aynı sıcaklıktaki iki maddeden, öz ısısı büyük olan madde, ısı enerjisi fazla olduğundan, çevresine daha fazla ısı enerjisi yayar.
Öz Isı, Sıcaklık Ve Kütle
Eşit miktarlarda su ve alkol, bir süre ısıtıldıklarında, ölçülen sıcaklıklarının birbirinden farklı olduğu görülür. Öz ısı, bir maddenin 1 gramının sıcaklığını 1°C arttırmak için gereken ısı miktarı olduğuna göre, öz ısısı büyük olan maddelerin sıcaklık artışı az, öz ısısı küçük olan maddelerin sıcaklık artışı fazla olmaktadır.
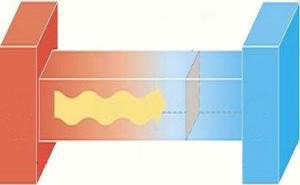 Bir kaptaki su ısıtılmaya başlandığında, belirli bir süre sonra suyun sıcaklığında bir artış olacaktır. Bu, ısıtmanın ve maddedeki sıcaklık değişiminin doğru orantılı olduklarını kanıtlar. Eşit miktarda (kütlede) ve eşit sıcaklıkta olan, örneğin su ve zeytinyağı, özdeş ısıtıcılarla ısıtıldığında, suyun öz ısısı (4,18) zeytinyağının öz ısısından (1,96) büyük olduğundan, sıcaklık artışlarının eşit olması isteniyorsa, öz ısısı daha büyük olan suyun daha uzun süre ısıtılması gereklidir.
Bir kaptaki su ısıtılmaya başlandığında, belirli bir süre sonra suyun sıcaklığında bir artış olacaktır. Bu, ısıtmanın ve maddedeki sıcaklık değişiminin doğru orantılı olduklarını kanıtlar. Eşit miktarda (kütlede) ve eşit sıcaklıkta olan, örneğin su ve zeytinyağı, özdeş ısıtıcılarla ısıtıldığında, suyun öz ısısı (4,18) zeytinyağının öz ısısından (1,96) büyük olduğundan, sıcaklık artışlarının eşit olması isteniyorsa, öz ısısı daha büyük olan suyun daha uzun süre ısıtılması gereklidir.
Biri tam dolu, diğeri yarısına kadar dolu iki kapta ısıtılan suyun, sıcaklıklarının belirli bir dereceye yükseltilmesi için, daha fazla miktarda olanının daha uzun süreyle ısıtılması gerekir. Bir maddenin aldığı ısı enerjisi o maddenin miktarına bağlıdır. Sıcaklık artışı ise maddenin miktarıyla (kütlesiyle) ters orantılıdır. Dolayısıyla, kütlesi fazla olan su daha az, kütlesi az olan su daha çok ısınır.
Kaynakça:
– C. Kittel, H. Kroemer, “Thermal Physics”, 2nd ed., W.H. Freeman, San Francisco,
Yazar: Oben Güney Saraçoğlu

Süper yazı gerçekten bir harika tebrik ederim