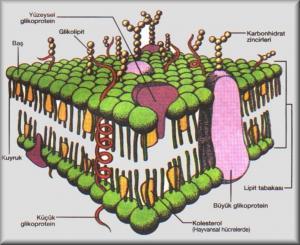
 Hücre zarının işlevselliğini kavrayabilmek için bir zarla iki yarıma ayrılan bir odacık hayal edelim. Daha da fazlası bazı madde parçacıklarının zardan geçebildiğini bazılarının ise geçemediğini farz edelim. Böyle bir zara farklı özellikte geçirgen (ya da seçici geçirgen) denir. Odacığın iki yarım kısmı arasında madde difüzyonu zarı nasıl etkileyecektir? Odacığın seçici geçirgen bir zarla bölünmüş U şeklinde bir tüp olduğunu farz edelim. A kısmında saf su, B kısmında ise aynı miktarda şeker çözeltisi (suda çözünmüş şeker) bulunsun. Her iki taraf da aynı başlangıç sıcaklığıyla ve basıncıyla karşı karşıya bulunsun. Eğer zar, suya geçirgen; ama şekere geçirgen değilse su molekülleri A’dan B’ye ve B’den A’ya olmak üzere her iki yönde zardan geçebilecektir.
Hücre zarının işlevselliğini kavrayabilmek için bir zarla iki yarıma ayrılan bir odacık hayal edelim. Daha da fazlası bazı madde parçacıklarının zardan geçebildiğini bazılarının ise geçemediğini farz edelim. Böyle bir zara farklı özellikte geçirgen (ya da seçici geçirgen) denir. Odacığın iki yarım kısmı arasında madde difüzyonu zarı nasıl etkileyecektir? Odacığın seçici geçirgen bir zarla bölünmüş U şeklinde bir tüp olduğunu farz edelim. A kısmında saf su, B kısmında ise aynı miktarda şeker çözeltisi (suda çözünmüş şeker) bulunsun. Her iki taraf da aynı başlangıç sıcaklığıyla ve basıncıyla karşı karşıya bulunsun. Eğer zar, suya geçirgen; ama şekere geçirgen değilse su molekülleri A’dan B’ye ve B’den A’ya olmak üzere her iki yönde zardan geçebilecektir.
Seçici geçirgen bir zar arasından çözücünün (genellikle su) bu hareketine osmoz denir. Biyolojik zarlar seçici geçirgendir ve bunların arasından suyun hareketi osmoz temeline bağlı olarak gerçekleşir. Küçük yağda çözünen moleküller gibi bazı çözünen maddeler de biyolojik zarlardan kolayca geçerler. Su, U-şeklindeki tüpün içindeki zarın her iki tarafında bulunduğundan, ilk önce zardan geçen su moleküllerinin her hangi bir belirgin etkisi olmadığı görülebilir. Fakat, şeker çözeltisi ve saf su arasındaki farklılığı daha dikkatli düşününüz. Maddelerin yüksek konsantrasyonlu bölgelerden düşük konsantrasyonlu bölgelere diffüze olduğu açıktır. A tarafında daha konsantrasyonlu bulunan su B tarafına geçmeye meyillidir; şeker molekülleri ise bir tarafa geçemeyip, B kısmında zar ile tutulurlar.
Su moleküllerinin neden A’dan B’ye geçtiğini zarın kendi üzerindeki olayları resimleyerek de görebiliriz. A tarafında verilen bir zaman aralığında zara vuracak tüm moleküller su molekülleridir ve zar suya geçirgen olduğundan, su moleküllerinin çoğu zar aracılığıyla A’dan B’ye geçecektir. Bunun tersine, B tarafında, aynı zaman aralığında zara vuran moleküllerin bazıları zardan geçebilen su molekülleri, bazıları ise zardan geçemeyen şeker molekülleri olacaktır. Çünkü zar, şeker moleküllerine geçirgen değildir. O zaman, her hangi bir verilen örnekte B yüzündeki zar kanallarının bazıları şeker molekülleri ile ilişki halindeyken bazıları su ile ilişkili olacaktır, halbuki A yüzünde kanallara giren tüm moleküller su molekülleridir. Her birim zamanda, A tarafından B tarafına zıt yönden daha fazla su molekülü zarı geçeceğinden; net osmoz da A’dan B’ye doğru olacaktır.
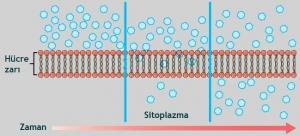 Meseleyi daha kısa bir şekilde entropi açısından da düşünebiliriz. Saf sudaki su moleküllerinin yerleşimi çok düzenlidir. Öyle ki, her bir moleküler bölge bir su molekülü ile doldurulmuştur. Halbuki yerleşim şeker çözeltisinde düzenli değildir. Burada bulunan her moleküler bölge ya su molekülü ya da şeker molekülü ile doldurulmuştur.
Meseleyi daha kısa bir şekilde entropi açısından da düşünebiliriz. Saf sudaki su moleküllerinin yerleşimi çok düzenlidir. Öyle ki, her bir moleküler bölge bir su molekülü ile doldurulmuştur. Halbuki yerleşim şeker çözeltisinde düzenli değildir. Burada bulunan her moleküler bölge ya su molekülü ya da şeker molekülü ile doldurulmuştur.
Düzenli sistemlerde düzensiz sistemlerden daha fazla serbest enerji bulunur. Burada da saf sudaki (A tarafı) düzenli su molekülleri, şeker çözeltisindeki (B tarafı) düzensiz su moleküllerinden daha fazla serbest enerjiye sahiptirler. A tarafından B’ye doğru su molekülleri için bir serbest-enerji gradiyenti vardır. Difüzyon ile ilgili genellememize göre, bu gradiyenti A’dan B’ye düşüren şey suyun net hareketi olacaktır. Belki de U-şeklindeki tüp içinde olan biteni hatırlamanın en kolay yolu, difüzyondaki genel kuralı yeniden anımsamak ve onu bu duruma uygulamaktır: Su, yüksek su konsantrasyonlu bölgeden (yani saf su) düşük su konsantrasyonlu bölgeye doğru hareket eder.
Artık şimdi, bazı ek genellemeler yapılabilecek durumdayız. Eğer osmotik açıdan aktif maddeler (çözünen ya da kolloyidal olarak dağılan parçacıklar) suda bulunuyorsa, su moleküllerinin serbest enerjisi sürekli düşer (Kolloyidal parçacıklar genellikle çözünmüş bir maddenin ayrılmış tek tek moleküllerinden daha büyüktür. Gerçek bir süspansiyonun büyük parçacıklarına benzemeksizin, tahmin edilebilir oranlarda bulunmayıp sıvı ortam içinde yayılmış şekilde yer alırlar). Bir sıvının osmotik konsantrasyonu “birim hacim için osmotik açıdan aktif parçacıkların sayısı” sıvının serbest enerjisiyle doğrudan bir ilişkiye sahiptir. U şeklindeki tüp örneğinde, su moleküllerinin serbest enerjisindeki düşme osmotik konsantrasyonla orantılıdır. Serbest enerjideki azalmanın nedeni, osmotik olarak aktif parçacıkların, su moleküllerinin düzenli üç-boyutlu çizgilerini bir miktar bozmalarıdır.
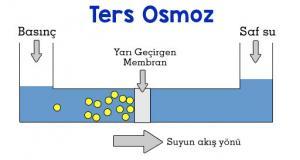
O zaman, osmotik konsantrasyonuna bağlı olarak her çözelti belirli bir serbest enerjiye sahiptir. Sabit sıcaklık ve basınç koşulları altında, bu serbest enerji hesaplanabilir; buna osmotik potansiyel denir. (Saf suyun osmotik potansiyel değeri sıfırdır. Osmotik konsantrasyon artarken osmotik potansiyel düşer. Tüm çözeltilerin sıfırdan daha düşük değerleri vardır). Eğer iki farklı çözelti yalnız suya geçirgen bir zarla birbirinden ayrılırsa, sıcaklık ve basınç da sabit kaldığında, suyun net hareketi düşük osmotik konsantrasyonlu çözeltiden yüksek osmotik konsantrasyonlu çözeltiye doğru olacaktır. Ne kadar yüksek osmotik konsantrasyon gradiyenti olursa, o kadar hızlı hareket olur.
Su, osmotik potansiyeldeki farklılık derecesi hız oranında yüksek osmotik potansiyelli bölgeden düşük potansiyelli bölgeye akar.
1. Osmotik olarak aktif maddeler (çözünmüş ya da kolloyidal olarak dağılmış parçacıklar) suda bulunuyorsa, su moleküllerinin serbest enerjisi sürekli azalır.
2. Su moleküllerinin serbest enerjilerindeki azalma osmotik konsantrasyon ile orantılıdır.
3. Suyun net hareketi, düşük osmotik konsantrasyonlu çözeltiden yüksek osmotik konsantrasyonlu çözeltiye doğru olacaktır.
U-şeklindeki tüpte suyun net hareketi A tarafından B’ye doğru ise, sıvının hacmi B tarafında artacak, A tarafında ise azalacaktır. Seçici geçirgenlik özelliği bu işlemin belirsiz bir süre devam etmesine mi yol açacak yoksa bir denge noktasına ulaşılabilinecek mi? Açıkca, durduracaktır. Niçin? Kuşkusuz, sıvı kolonu yerçekimi kuvvetiyle aşağıya doğru çekilir. Kolon yükseldiği için, bunun ağırlığı hidrostatik basıncın aşağıya doğru artmasını güç sarfederek sağlar. Basınç arttığı için, şeker çözeltisindeki suyun serbest enerjisi yükselir; çünkü basıncın kendisi de bir serbest enerji (yararlı enerji) şeklidir. Sonuçta şeker çözeltisinin kolonu öyle yükselir, basıncı ve serbest enerjisi öyle büyür ki su molekülleri A’dan B’ye geçerken sahip oldukları kadar hızlı bir şekilde B’den A’ya aradaki zardan itilerek geçerler.
Su aynı hızda; ama ters yönde zardan geçerken sistem serbest enerjisiyle ve osmotik potansiyeliyle dinamik denge içindedir. Yani, zarın bir tarafında serbest enerjili saf su, diğer tarafında ise kolonun osmotik potansiyeli ve hidrostatik basıncı bulunur. Açıkça, zarın karşısındaki daha büyük değişim farklılığı, iki taraf arasındaki osmotik potansiyeldeki daha büyük farklılık ve çözelti kolonunun da yüksekliği, bu farklılığın hidrostatik basınçtaki değişiklikle denkleşmesinden önce yükselecektir.
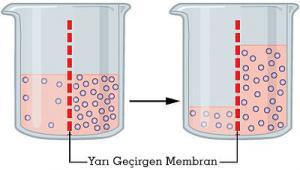 Osmotik konsantrasyonun ağırlıkça bir konsantrasyon olmadığını; fakat moleküler ya da iyonik konsantrasyondan çok, her bir birim hacim için çözünen parçacıkların toplam sayısı olduğunu bilmek önemlidir. Eğer aynı çözelti içinde birkaç çeşit çözünen madde varsa, o zaman o çözeltinin osmotik konsantrasyonu tüm çeşitli parçacıkların hepsinin toplamı (her birim hacim için) ile tespit edilir.
Osmotik konsantrasyonun ağırlıkça bir konsantrasyon olmadığını; fakat moleküler ya da iyonik konsantrasyondan çok, her bir birim hacim için çözünen parçacıkların toplam sayısı olduğunu bilmek önemlidir. Eğer aynı çözelti içinde birkaç çeşit çözünen madde varsa, o zaman o çözeltinin osmotik konsantrasyonu tüm çeşitli parçacıkların hepsinin toplamı (her birim hacim için) ile tespit edilir.
Eğer çözünen bir madde iyonize olursa osmoz bakımından her biri farklı bir parçacık olarak işlev görür. Suda çözünen bir mol sodyum klorit (NaC1) iki mol parçacık oluşturur. Na+ iyonları ve iyonları. Kolloyidal parçacıklar toplam osmotik konsantrasyona da katılırlar.
Kaynakça:
Khan Academy
Yazar: Taner Tunç
