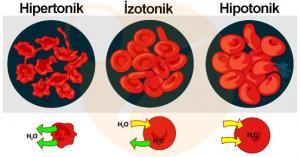
 Hücre zarı yaşamı oluşturmak için bir araya gelen tüm organik kimyasalları bir arada tutan bir torbadan biraz daha farklı bir yapıdadır. Hücre zarı, hücreye şekil ve mekanik güç veren pasif bir zardan çok daha ayrıntılı yapıya sahiptir. Hücre hareketine ve hücrenin dış devresiyle ilişkisine duyarlıdır. Daha da fazlası, hücrenin son derece düzenli içi ve potansiyel olarak yıkıcı dış çevresi arasındaki kimyasal madde trafiğinin düzenlenmesi için birinci derecede sorumluluk taşır. Bir hücrenin içine ve dışına girip çıkan tüm maddeler bir zar engelinden geçmelidir ve her bir hücrenin zarı neyi, hangi hızla ve hangi yönde geçireceğine tam özgül olmalıdır. Hücre zarı bu kontrolü iki şekilde yapar:
Hücre zarı yaşamı oluşturmak için bir araya gelen tüm organik kimyasalları bir arada tutan bir torbadan biraz daha farklı bir yapıdadır. Hücre zarı, hücreye şekil ve mekanik güç veren pasif bir zardan çok daha ayrıntılı yapıya sahiptir. Hücre hareketine ve hücrenin dış devresiyle ilişkisine duyarlıdır. Daha da fazlası, hücrenin son derece düzenli içi ve potansiyel olarak yıkıcı dış çevresi arasındaki kimyasal madde trafiğinin düzenlenmesi için birinci derecede sorumluluk taşır. Bir hücrenin içine ve dışına girip çıkan tüm maddeler bir zar engelinden geçmelidir ve her bir hücrenin zarı neyi, hangi hızla ve hangi yönde geçireceğine tam özgül olmalıdır. Hücre zarı bu kontrolü iki şekilde yapar:
1. Difüzyon gibi doğal olayları gerçekleştirerek,
2. Belirli maddeleri içeri ya da dışarı geçirerek.
Difüzyon
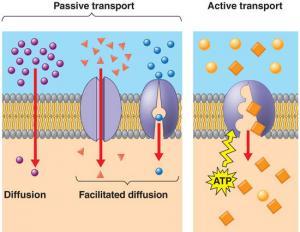 Sıcaklık söz konusu moleküllerin kinetik enerjilerini arttırarak kimyasal tepkimelerin hızını etkiler. İçinde, bir köşesinde toplu halde 17 tane bilya bulunan, duran bir kutu düşünün. Kutuyu salladığımızda, bilyalar kutunun dibinde her yöne yayılır. Bu sonuçtan belirgin bir şekilde görüldüğü gibi, olayla daha yakından ilgilenmeye değer; çünkü bilyalar moleküller şeklinde, sallama ise sisteme kinetik enerji ya da ısı enerjisi katmak şeklinde düşünülebilir. Bir bilyanın hareket edebileceği tüm olası yönler çok belirgindir. Bunlar bilyaların oluşturduğu kümenin merkezinden öne doğru bir hareket şeklindedir. Çünkü rastgele hareket bilya kümesini korumadan daha çok dağıtmaya neden olur. 3. bölümde belirttiğimiz gibi, herhangi bir karşı dış etki yokluğunda, dinamik bir sistem daha az olası düzenli durum yerine daha çok olası düzensiz duruma doğru hareket edecektir. Bu durum tamamen beklenen şeydir. Örnegin, bir kesme şeker sıcak bir fincan kahve içinde çözündüğü zaman: şeker molekülleri şeker kristallerinin yüksek konsantrasyonlu bulundukları bölgeden daha düşük konsantrasyonlu bölgeye doğru hareket ederler. Sonunda, şeker molekülleri sıvının içinde tamamen dağılmış olur.
Sıcaklık söz konusu moleküllerin kinetik enerjilerini arttırarak kimyasal tepkimelerin hızını etkiler. İçinde, bir köşesinde toplu halde 17 tane bilya bulunan, duran bir kutu düşünün. Kutuyu salladığımızda, bilyalar kutunun dibinde her yöne yayılır. Bu sonuçtan belirgin bir şekilde görüldüğü gibi, olayla daha yakından ilgilenmeye değer; çünkü bilyalar moleküller şeklinde, sallama ise sisteme kinetik enerji ya da ısı enerjisi katmak şeklinde düşünülebilir. Bir bilyanın hareket edebileceği tüm olası yönler çok belirgindir. Bunlar bilyaların oluşturduğu kümenin merkezinden öne doğru bir hareket şeklindedir. Çünkü rastgele hareket bilya kümesini korumadan daha çok dağıtmaya neden olur. 3. bölümde belirttiğimiz gibi, herhangi bir karşı dış etki yokluğunda, dinamik bir sistem daha az olası düzenli durum yerine daha çok olası düzensiz duruma doğru hareket edecektir. Bu durum tamamen beklenen şeydir. Örnegin, bir kesme şeker sıcak bir fincan kahve içinde çözündüğü zaman: şeker molekülleri şeker kristallerinin yüksek konsantrasyonlu bulundukları bölgeden daha düşük konsantrasyonlu bölgeye doğru hareket ederler. Sonunda, şeker molekülleri sıvının içinde tamamen dağılmış olur.
Sıvı ne kadar sıcak olursa, çözelti içindeki moleküller de daha fazla kinetik enerjiye sahip olurlar. Bu sayede difüzyon da daha hızlı gerçekleşir. Tartışmanın istatistiksel olduğuna dikkat ediniz. Rastgele hareketin bir sonucu olarak, dağılan tüm 17 bilyanın kutunun bir köşesinde bir küme oluşturma olasılığı da vardır. Bu sonucun belirgin bir meydana gelme olasılığı vardır; fakat önemsenmeyen bir olasılık da haklı bir şekilde ihmal edilebilir. Burada kullanılan sonuçlanma tipi tamamen tipik bir bilimsel sonuçlanmadır: bilimin gerçekleri ve kanunları değer yargılarından daha çok istatistikseldir. Onlar, olası sonuçlara dayanarak doğal olayları tanımlarlar; zamanın yüzde yüzünde oluşacak kesin bir sonuç üzerinde durmazlar.
Şimdi, kutu içindeki bilyalar örneğine ya da buna benzeyen diğer örneklere dayanarak bir genelleme yapabiliriz: Diğer tüm faktörlerin eşit olduğu durumda özel bir maddenin parçacıklarının net hareketi o maddenin daha yüksek konsantrasyonlu bölgesinden daha düşük konsantrasyonlu bölgesine doğrudur. Dikkat edilirse burada net hareketten söz ediyoruz. Her zaman ters yönde hareket eden bazı parçacıklar olacaktır; fakat özünde, hareket konsantrasyon merkezinden uzaklara doğru olacaktır. Verilen bir maddenin parçacıklarının uygun alan içinde bir diğerinden nispeten eşit uzaklıkta olmaya meyilli olması belirli bir sonuçtur. Bu durumda homojen yoğunluğa ulaşıldığı zaman, sistem dengededir; parçacıklar hareket etmeye devam ederler; fakat sistemde küçük net değişiklik vardır.
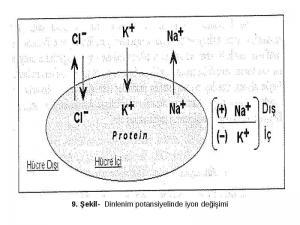 Moleküllerin boyutuna bağlı olarak parçacıkların bir yerden diğer bir bölgeye hareketine tartışmakta olduğumuz şekilde difüzyon denir. Difüzyon gazlarda, belirgin bir şekilde en hızlıdır; çünkü parçacıklar arasında daha çok alan bulunur ve bu yüzden de hareketin gecikmesine yol açan nispeten küçük bir çarpışma şansına sahiptir. Sıvı içindeki difüzyon daha yavaştır. Konveksiyon akımlarının olmadığı zaman bir madde soğuk su içinde yalnız bir metrelik mesafeyi bir kaç yıl gibi çok uzun zamanda alabilir. Katılar içindeki difüzyon kuşkusuz çok daha yavaştır: Bir katı maddenin molekülleri arasında çok küçük alan vardır ve çarpışmalar, moleküller hareket almadan hemen önce gerçekleşir.
Moleküllerin boyutuna bağlı olarak parçacıkların bir yerden diğer bir bölgeye hareketine tartışmakta olduğumuz şekilde difüzyon denir. Difüzyon gazlarda, belirgin bir şekilde en hızlıdır; çünkü parçacıklar arasında daha çok alan bulunur ve bu yüzden de hareketin gecikmesine yol açan nispeten küçük bir çarpışma şansına sahiptir. Sıvı içindeki difüzyon daha yavaştır. Konveksiyon akımlarının olmadığı zaman bir madde soğuk su içinde yalnız bir metrelik mesafeyi bir kaç yıl gibi çok uzun zamanda alabilir. Katılar içindeki difüzyon kuşkusuz çok daha yavaştır: Bir katı maddenin molekülleri arasında çok küçük alan vardır ve çarpışmalar, moleküller hareket almadan hemen önce gerçekleşir.
Tüm bu örneklerde, difüzyon hızını önemsemeden tüm bölgelerde aynı sıcaklık ve basınç altında, net etki yüksek konsantrasyonlu bölgelerden diğer bölgelere doğru olan harekettir. Moleküllerin genel olarak ılık sulu çözeltilerde bulunduğu ve üzerinde durulan mesafelerin bir milimetrenin kesirleri şeklinde olan canlı organizmalarda, difüzyon, son derece önemli bir olaydır. Öyle ki, bir amino asit ya da bir nükleotit sulu bir ortamda 0,5 saniyeden daha az zamanda bir hücrenin çapı (10-50 mikron) kadar difüze olur.
Şimdiye kadar, yüksek konsantrasyonlu bölgeden düşük konsantrasyonlu bölgeye hareketle ilgili olarak difüzyon üzerinde durduk. Ancak, canlılar dünyasında difüzyon tam olarak bir konsantrasyon işlevi değildir; çünkü yaşamla ilgili olayların gerçekleştikleri yerlerde koşullar nadiren sabittir. İşte bu yüzden, üzerinde durulan parçacıkların serbest enerjisiyle ilgili olarak difüzyona bakmak bizim için çok yararlı olacaktır. Bir maddenin bölgesel konsantrasyonu nispeten düzgün ve olasılıksız olarak düzenlidir. Örnegin, şeker moleküllerinin ve kahvenin orijinal küp şeker ve tatlandırılmamış kahveye geri dönmesi gibi bir değişiklik için bir enerjiye gereksinim olduğunu görebiliriz. Moleküllerin rastgele ve düzensiz sıralanması iş yapmak için düzenli halinden daha az potansiyele gereksinim gösterir ve aynı zamanda da daha az serbest enerjiye sahiptir.
Bir sistemdeki düzensizlik miktarı entropi olarak bilinir. Termodinamiğin 2. kanunundan bildiğimiz gibi evrendeki serbest enerji miktarı sürekli azalmaktadır, entropi ise artmaktadır. Difüzyon, o zaman, birarada konsantre olan düzenli moleküllerin yayılan moleküllerden daha büyük serbest enerjiye sahip olmaları yüzünden kendi kendine olan bir olaydır. Yani düzenlilikten düzensizliğe doğru olan bir azalma tepkimesidir. Karışım (ya da ürün) ayrı orjinal maddelerden (reaktantlar) daha az serbest enerjiyi sahiptir.
 Eğer iki saf maddeyle başlarsak, difüzyon hızı başlangıçta en hızlıdır ve tam karışım dengesine ulaşıldığında yavaşlar. Eğer moleküler düzeyde bir difüzyon gözlemleyebilseydik, tepkimenin ilk başlarında küp şekerden uzaklaşan şeker moleküllerini görebilirdik. Daha sonra, madde çok daha fazla karıştığı için, şeker moleküllerini çözmekte olan küp şekere götürecek geri tepkimenin sıklığı da, dengeye ulaşılana kadar, yükselecekti. Difüzyon bu durumda, içerdiği maddelerin özelliğine bağlı olan kendi serbest enerjisiyle meydana gelen bir kimyasal tepkimedir.
Eğer iki saf maddeyle başlarsak, difüzyon hızı başlangıçta en hızlıdır ve tam karışım dengesine ulaşıldığında yavaşlar. Eğer moleküler düzeyde bir difüzyon gözlemleyebilseydik, tepkimenin ilk başlarında küp şekerden uzaklaşan şeker moleküllerini görebilirdik. Daha sonra, madde çok daha fazla karıştığı için, şeker moleküllerini çözmekte olan küp şekere götürecek geri tepkimenin sıklığı da, dengeye ulaşılana kadar, yükselecekti. Difüzyon bu durumda, içerdiği maddelerin özelliğine bağlı olan kendi serbest enerjisiyle meydana gelen bir kimyasal tepkimedir.
Difüzyonu anlamada serbest enerji, konsantrasyon gradiyentinden daha geniş uygulanabilir bir kaynaktır. Bir yönde hafif bir konsantrasyon gradiyenti, aksi yönde sıcaklı k gradiyentinin olduğu bir düzenek düşününüz. Bu iki gradiyentin birbirlerine karşı etkileri iki gradiyentin nispi serbest enerjilerine tamamen bağımlı olan moleküllerin net hareketini yapar. Bu hareket, bu durumda yüksek sıcaklık bölgesinden daha yüksek konsantrasyonlu bölgeye doğru olur.
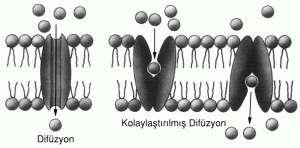 Hücrelerle ilişkili olarak difüzyonun önemi ve serbest enerjideki esas prensipleri açıktır: Organik moleküllerin konsantrasyonu ve bir hücre içinde seçilmiş bir iyon grubu çok düzensiz bir yerleşim gösterir. Hücre zarı olmaksızın, hücre kimyasının serbest enerjisi çevreye yayılan hücre içeriği şeklinde kaybolacaktır. Buradan iki sonuç çıkmaktadır. Birincisi, hücrenin içi ve dışı arasında, hücre kimyasının bütünlüğünün sağlanması için bir engel olmalıdır. İkincisi, ise hücre zarının her iki yanındaki serbest enerji gradiyenti işlemeye uygun olmalıdır.
Hücrelerle ilişkili olarak difüzyonun önemi ve serbest enerjideki esas prensipleri açıktır: Organik moleküllerin konsantrasyonu ve bir hücre içinde seçilmiş bir iyon grubu çok düzensiz bir yerleşim gösterir. Hücre zarı olmaksızın, hücre kimyasının serbest enerjisi çevreye yayılan hücre içeriği şeklinde kaybolacaktır. Buradan iki sonuç çıkmaktadır. Birincisi, hücrenin içi ve dışı arasında, hücre kimyasının bütünlüğünün sağlanması için bir engel olmalıdır. İkincisi, ise hücre zarının her iki yanındaki serbest enerji gradiyenti işlemeye uygun olmalıdır.
Kaynakça:
Khan Academy
Yazar: Taner Tunç
