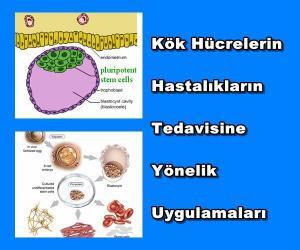
 Çok sayıda ilaç, yeni tanı prosedürleri ve karmaşık cerrahi müdahaleler gibi modern tıbbi teknolojiler dünyanın birçok yerinde insanların yaşam süresini uzatmaktadır. Diğer taraftan, kronik ve yaşa bağlı hastalıkların artması, yaşam şekli ile ilgili hastalıklar ya da çevre kirliliğinin neden olduğu hastalıklar, tıbbi araştırmaların ilgilendiği yeni alanlardır. Bu nedenle, güncel ve onarıcı yeni tedavi yöntemlerine ihtiyaç duyulmaktadır.Kök hücreye dayalı yöntemler de yenilikçi tedavi metotları olarak geliştirilmeye çalışılmaktadır. Vücutta belirli bir hücre tipine özelleşmiş olan hücrelerin aksine, farklılaşmamış, çoğalabilen ve farklı hücre tiplerine dönüşebilme potansiyeline sahip hücrelere kök hücre denir. Bu özellikleri nedeniyle kök hücrelerin, vücutta artmış hücre ölümüne neden olan çeşitli hastalıklarda bir tedavi yöntemi olarak kullanılması gündeme geldi.
Çok sayıda ilaç, yeni tanı prosedürleri ve karmaşık cerrahi müdahaleler gibi modern tıbbi teknolojiler dünyanın birçok yerinde insanların yaşam süresini uzatmaktadır. Diğer taraftan, kronik ve yaşa bağlı hastalıkların artması, yaşam şekli ile ilgili hastalıklar ya da çevre kirliliğinin neden olduğu hastalıklar, tıbbi araştırmaların ilgilendiği yeni alanlardır. Bu nedenle, güncel ve onarıcı yeni tedavi yöntemlerine ihtiyaç duyulmaktadır.Kök hücreye dayalı yöntemler de yenilikçi tedavi metotları olarak geliştirilmeye çalışılmaktadır. Vücutta belirli bir hücre tipine özelleşmiş olan hücrelerin aksine, farklılaşmamış, çoğalabilen ve farklı hücre tiplerine dönüşebilme potansiyeline sahip hücrelere kök hücre denir. Bu özellikleri nedeniyle kök hücrelerin, vücutta artmış hücre ölümüne neden olan çeşitli hastalıklarda bir tedavi yöntemi olarak kullanılması gündeme geldi.
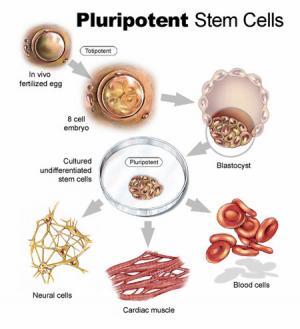
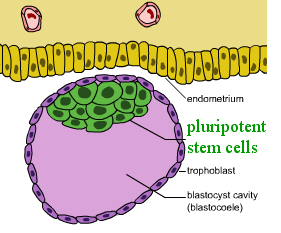
 Kök hücrelerin, farklı hücre tiplerine özelleşebilme yeteneğine göre çeşitli türleri vardır. Tedaviye yönelik uygulamalar da kök hücrelerin türleri ile ilişkilidir. Spermin yumurtayı döllemesi sonucunda oluşan zigot bir hücre bölünmesi geçirir. Bölünme sonucunda iki tane hücre ortaya çıkar. Bu her iki hücreye totipotent kök hücre denir ve bu hücreler tek başına bir organizmayı oluşturabilecek kapasitededir. Bu aşamadan sonra, hücreler bölünmeye devam eder ve blastokist denilen bir gelişim evresine ulaşır. Bu evrede, iki katlı hücre tabakasının iç kısmında bir hücre yığını oluşur. Bu hücre yığınındaki hücrelere, pluripotent kök hücreler denir. Pluripotent kök hücrelerin özelliği, belirli koşullarda vücutta her organdaki spesifik hücre türlerine farklılaşabilmeleridir. Örneğin; uygun koşullarda, bir pluripotent hücre, kemik hücresine, kas hücresine, sinir hücresine ya da başka hücre tiplerine farklılaşabilir. Organizmaların vücudunda bulunan ve sadece bulunduğu organa özgü belirli hücre türlerine özelleşebilen hücrelere ise multipotent kök hücreler denir. Hastalıkların tedavisinde, pluripotent hücrelerin kullanımı yeni bir yaklaşım olarak ortaya çıkmıştır. Fakat, pluripotent kök hücrelerin sadece embriyolardan elde edilmesi mümkündü. Bu nedenle, embriyonik kök hücrelerin kullanımının etik olup olmayacağı tartışmaları gündeme gelmiştir.
Kök hücrelerin, farklı hücre tiplerine özelleşebilme yeteneğine göre çeşitli türleri vardır. Tedaviye yönelik uygulamalar da kök hücrelerin türleri ile ilişkilidir. Spermin yumurtayı döllemesi sonucunda oluşan zigot bir hücre bölünmesi geçirir. Bölünme sonucunda iki tane hücre ortaya çıkar. Bu her iki hücreye totipotent kök hücre denir ve bu hücreler tek başına bir organizmayı oluşturabilecek kapasitededir. Bu aşamadan sonra, hücreler bölünmeye devam eder ve blastokist denilen bir gelişim evresine ulaşır. Bu evrede, iki katlı hücre tabakasının iç kısmında bir hücre yığını oluşur. Bu hücre yığınındaki hücrelere, pluripotent kök hücreler denir. Pluripotent kök hücrelerin özelliği, belirli koşullarda vücutta her organdaki spesifik hücre türlerine farklılaşabilmeleridir. Örneğin; uygun koşullarda, bir pluripotent hücre, kemik hücresine, kas hücresine, sinir hücresine ya da başka hücre tiplerine farklılaşabilir. Organizmaların vücudunda bulunan ve sadece bulunduğu organa özgü belirli hücre türlerine özelleşebilen hücrelere ise multipotent kök hücreler denir. Hastalıkların tedavisinde, pluripotent hücrelerin kullanımı yeni bir yaklaşım olarak ortaya çıkmıştır. Fakat, pluripotent kök hücrelerin sadece embriyolardan elde edilmesi mümkündü. Bu nedenle, embriyonik kök hücrelerin kullanımının etik olup olmayacağı tartışmaları gündeme gelmiştir.
 Kök hücreye dayalı uygulamalar umut verici olarak değerlendirilir. Fakat, multipotent kök hücrelerin kalp dokusunu onarmada kullanıldığı en son deneysel ve klinik çalışmaların sonuçları hayal kırıklığı yaratmıştır. Çünkü bu çalışmaların sonucunda, kalp dokusunda herhangi bir işlevsel düzelme görülmemiştir. Multipotent kök hücrelerin uygulanmasındaki ana kısıtlayıcı faktör, laboratuvar ortamında çoğalmalarının ve başka hücre tiplerine farklılaşmalarının sınırlı olmasıdır. Oysa, multipotent kök hücrelerin kemik dokusu ve dolaşım sistemi ile ilgili uygulamalarının başarılı olduğu gösterilmiştir. Fakat, beyin ve kalp gibi yenilenme potansiyeli daha az olan organları etkileyen hastalıklarda, tedavi edici etkileri görülmemiştir. Multipotent kök hücrelerin kullanılmasıyla ilgili diğer bir kısıtlayıcı durum, bu hücrelere tedavi edici genlerin aktarılması ve çoğaltılmasındaki sınırlamalardır. Bu nedenle, tedavi için pluripotent kök hücrelere yönelik çalışmalar artmıştır.
Kök hücreye dayalı uygulamalar umut verici olarak değerlendirilir. Fakat, multipotent kök hücrelerin kalp dokusunu onarmada kullanıldığı en son deneysel ve klinik çalışmaların sonuçları hayal kırıklığı yaratmıştır. Çünkü bu çalışmaların sonucunda, kalp dokusunda herhangi bir işlevsel düzelme görülmemiştir. Multipotent kök hücrelerin uygulanmasındaki ana kısıtlayıcı faktör, laboratuvar ortamında çoğalmalarının ve başka hücre tiplerine farklılaşmalarının sınırlı olmasıdır. Oysa, multipotent kök hücrelerin kemik dokusu ve dolaşım sistemi ile ilgili uygulamalarının başarılı olduğu gösterilmiştir. Fakat, beyin ve kalp gibi yenilenme potansiyeli daha az olan organları etkileyen hastalıklarda, tedavi edici etkileri görülmemiştir. Multipotent kök hücrelerin kullanılmasıyla ilgili diğer bir kısıtlayıcı durum, bu hücrelere tedavi edici genlerin aktarılması ve çoğaltılmasındaki sınırlamalardır. Bu nedenle, tedavi için pluripotent kök hücrelere yönelik çalışmalar artmıştır.
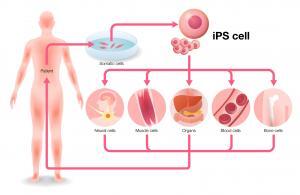
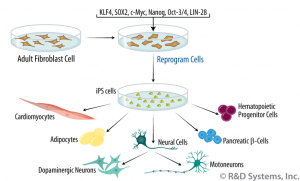
2012 yılında S. Yamanaka uyarılmış pluripotent kök hücrelerin hastalık modeli olarak kullanılmasıyla ilgili yaptığı çalışmalardan dolayı Nobel ödülü almıştır. Bu teknoloji, günümüzde hastalık modellemesi ve ilaç geliştirme alanlarında kullanılmaktadır. Yamanaka ve arkadaşlarının yaptığı çalışmada, bir hastanın derisinde bulunan fibroblast hücreleri alınmıştır. Bu hücrelere laboratuvar ortamında, Oct3/4, Sox2, Klf4 ve c-Myc genleri aktarılmıştır. Bu işlemden sonra hücreler pluripotent kök hücre karakteristiğini kazanmışlardır. Bu nedenle bu hücrelere uyarılmış pluripotent kök hücreler (iPSC) denir. Ayrıca, bu teknolojide hastanın kendi hücreleri kullanıldığı için, hücreler hastaya tekrar aktarıldığında bağışıklık sistemi yanıtı görülmez. Yöntemin diğer avantajı ise, embriyonik kök hücrelere gereksinimi ortadan kaldırmasıdır.
Japonya’da, makula dejenerasyonu hastası olan kişiler, uyarılmış pluripotent kök hücrelere dayalı tedavinin ilk defa uygulandığı hastalardı. Bu tedavide, iPSC hücrelerinden kökenlenen retinal pigment epitelyum dokusu hastalara aktarılmıştır. Tüm dünyada, makula dejenerasyonu, diyabet, kalp hastalıkları ve nörodejeneratif hastalıkların tedavisinde, iPSC kökenli tedaviler üzerine klinik çalışmalar devam etmektedir.
iPSC konusunda tüm dünyada yoğun araştırmalar devam etmektedir. Bu araştırmalar; uyarılmış pluripotent kök hücrelerde genetik mühendisliği uygulamalarını ve bu kök hücrelerin farklı hücre tiplerine dönüştürülmesi ile ilgili çalışmaları içermektedir. Klinik uygulamalar için, uyarılmış pluripotent hücrelerin hastalara naklinin güvenliği ile ilgili çalışmalar devam etmektedir.
iPSC Terapileri İçin Teknolojik Gereklilikler
Günümüze değin, embriyonik kök hücrelerin ve iPSC kullanımıyla ilgili pek çok teknik zorluğun üstesinden gelinmiştir. Uygun koşullar sağlanarak insan iPSC hücreleri biyoreaktörlerde üretilebilir. iPSC hücrelerinin genomunda değişiklik yapmak için CRISPR-Cas 9 gibi genom düzenleme yöntemleriyle protokoller geliştirildi. Genomda yapılacak değişiklik transgene aktarımını ya da hastalığa neden olan mutasyonun düzeltilmesini içermektedir.
iPSC’e dayalı hücresel terapiler için bir diğer zorluk, hücre aktarım yönteminin henüz yeterli şekilde tanımlanmamasıdır. Örneğin; kalp enfarktüsünden sonra, kalp dokusunun onarımı için kemik iliği hücreleri, koroner arter yoluyla aktarılmıştı. Bu yolla aktarılan hücreler başarılı bir şekilde kalp dokusuna ulaşmıştı ama kalp hücrelerine dönüşememişlerdi. iPSC türevli olan kalp hücreleri ameliyatla doğrudan kalp dokusuna aktarılır ya da katater kullanılır.
 iPSC Tedavisinin Riskleri
iPSC Tedavisinin Riskleri
En kritik nokta iPSC türevli hücrelerin aktarımında genetik anormalliklerin ortaya çıkması olasılığıdır. Bu noktada, kaynak olarak kullanılacak hücrelerde var olan mutasyonların tanımlanması önemlidir. Buna ek olarak, iPSC hücreleri klinik kullanımdan önce düzenli olarak kontrol edilir. Ayrıca, iPSC hücrelerinde bulunan genetik anormaliler tümör oluşumunu tetikleyebilir. Fakat vücutta da çok sayıda genetik anormali bulunan hücreler her zaman tümör oluşturmaz. Bu nedenle kök hücrelerde oluşan genetik anormalliklerin tümör oluşturacak özellikte olup olmadığının değerlendirilmesi gereklidir. Bu yüzden, hücreler aktarılmadan önce; karyotipleme, tüm ekzon dizileme gibi karmaşık analiz yöntemleri uygulanır.
İlgili doku, organ ve hasta ile ilgili riskler de vardır. Örneğin; iPSC türevli kalp hücrelerinin aktarılmasından sonra; ölümcül olan aritmi, donör hücrelerin ölmesinden kaynaklı olan iltihap ve bağışıklık sisteminin aktarılan hücrelere cevap vermesi gibi riskler vardır. iPSC’e dayalı tedaviler için tüm bu riskler değerlendirilmelidir.
iPSC’e dayalı hücresel tedavilerin klinikte rutin olarak uygulanabilmesi için, tedavi protokolleri için bir standardın oluşturulması gereklidir. Bunun için, kök hücrelerin çoğaltılacağı ve farklılaştırılacağı besiyerlerinin optimizasyonu yapılmıştır ve ticari olarak mevcuttur. Fakat, kök hücreleri genetik olarak programlamayı sağlayan kitler, geliştirilmeye devam edilmektedir. Ayrıca, kök hücrelerin genetik stabilitesi üzerinde daha fazla araştırma yapılmalıdır. Hücreler uygulanmadan önce risk değerlendirilmesi yapılmalıdır.
Göz Hastalıkları Tedavisinde iPSC Kullanımı
Günümüzde çok sayıda klinik deneme, iPSC’e dayalı tedavilerle makula dejenerasyonun tedavisini hedeflemektedir. Bu konuda, 20’den fazla embryonik kök hücreye dayalı denemeler; Çin, Brezilya, İsrail, Amerika Birleşik Devletleri, Kore ve Birleşik Krallık gibi çok sayıda ülkede gerçekleştirilmiştir. Bunlar arasında, tek bir deneme sonlanmıştır. Diğer denemeler günümüzde hala yeni hastalar üzerinde devam etmektedir. Eylül 2014’te Japonya’da, iPSC türevli retinalardan makula dejenerasyon tedavisi ilk defa uygulanmıştır. Transplantasyondan bir yıl sonra herhangi bir ciddi komplikasyon ve tumör oluşumuna neden olabilecek bir hücre çoğalmasına rastlanmamıştır. Bu şekilde tedavi edilen gözlerde herhangi bir doku reddi ve gözün kötüye gitmesi durumu gözlemlenmemiştir. Bu gelişmelerin sonucunda, iPSC hücrelerine dayalı transplantasyonun hastalara uygulanabileceği ve güvenli olduğu sonucuna varılmıştır.
 Nörolojik Hastalıkların Tedavisinde iPSC Kullanımı
Nörolojik Hastalıkların Tedavisinde iPSC Kullanımı
Hücresel terapi konusunda, dünyada endüstrinin sponsorluğu ile gerçekleştirilen ilk klinik deneme, 2010’da insan embriyonik kök hücreleri kullanılarak Kaliforniya’da gerçekleştirilmiştir. Bu projede, insan embriyonik kök hücrelerinin, omurilik hasarı durumunda sinirlerin tekrar gelişmesine yardım edip etmeyeceği incelenmiştir. 2017’de, bu yöntemle tedavi edilen 5 hastanın, herhangi bir bağışıklık sistem cevabı göstermediği tespit edilmiştir. Fakat nörolojik fonksiyonlarda herhangi bir değişiklik gözlemlenmemiştir. Bu çalışmaya ek olarak, Çin’de Parkinson Hastalığının tedavisi için, embriyonik kök hücrelere dayalı bir klinik çalışma başlatılmıştır.
Diyabet Tedavisinde iPSC Kullanımı
Diyabet tedavisi için 4 adet, endüstrinin sponsor olduğu klinik deneme gerçekleştirilmiştir. Bu denemelerde, embriyonik kök hücrelerden üretilmiş beta hücreleri kullanılmıştır. Bu pankreatik hücreler, hücreleri bağışıklık sistemi hücrelerine karşı koruyan bir cihaz yardımıyla hastalara aktarılmıştır.
iPSC hücrelerinden türevlenmiş hücrelerle yapılan tedavi yöntemleri, hastalarda bağışıklık sistemi yanıtı oluşturmadıkları için uygulanabilir gözükmektedir. Fakat, tedavinin uygulanması; hastadan iPSC hücrelerinin elde edilmesi, laboratuvar ortamında istenilen hücre tiplerine farklılaştırılması, genom düzenleme ve kalite kontrol süreçlerini içeren uzun süreli ve maliyetli bir işlemdir. Ayrıca, klinik uygulamaların FDA ya da EMA gibi ulusal otoritelerle birlikte geliştirilmesi gerekir.
Alternatif olarak, biyobankalarda iPSC hücreler depo edilebilir. Bu sayede, hastaların kullanımı için hastayla uyumlu HLA içeren hücreler kullanılabilir. Buna ek olarak, hücredeki HLA sistemi genetik olarak değiştirilebilir. Bu sayede, kullanılacak hastaya uyumlu hücreler oluşturulabilir. Fakat bu uygulamaların, rutin klinik işlemlere dönüştürülmesi için öncelikle hastalardaki bağışıklık sistemi yanıtının uzun süreli olarak gözlemlenmesi gerekmektedir.
- iPSC teknolojisi ile ilgili bahsedilen bu sorunlar aşıldığında, önümüzdeki yıllarda, iPSC’e dayalı tedavi yöntemlerinin çeşitli hastalıkların tedavisinde rutin olarak uygulanması mümkün olacaktır.Kaynakça:
1) Martin. Therapeutic Application of Pluripotent Stem Cells:
Challenges and Risks. doi: 10.3389/fmed.2017.00229.
Yazar:Ayça Olcay
