Retinal hastalıklar; kalıtımsal, geri dönüşü olmayan ve tedavi edilemeyen görüş kaybının en önemli sebebidir. Çeşitli kemirgenler üzerindeki hastalık modelleri bu konuda bilgi sağlarken; hastalıkla ilişkili dokunun yokluğu ve türle ilişkili farklılıklar, insanlarda görülen görme kaybını anlama konusunda en büyük engellerdir. İnsan pluripotent kök hücreleri (iPSC), hastalık mekanizmasını anlamak ve yeni potansiyel terapötik hedefler için yeni bir yol açar.
İnsan gözü vücuttaki en kompleks organlardan biridir ve farklı hücre tiplerindeki milyonlarca devreden oluşur. Ayrıca nöral retina, insan gözü için mükemmel bir model olarak görev yapar. Beyin fonksiyonlarının %30’undan fazlası, göz tarafından algılanan ışığı analiz eder. Göz, embriyonik gelişim sırasında nöroepitelyum adı verilen bir dokudan türevlenir.
Gözdeki retina yapısı temel olarak nöroretina ve retinal pigment epitelyum (RPE) hücrelerinden oluşur. Nöroretina çok katmanlıdır ve fotoreseptörlerden (çubuk ve koni adı verilen hücreler), retinal gangliyo hücrelerinden (RGC) ve internöronlardan oluşur. Fotoreseptörler en dış katmanı oluşturur. Fotoreseptörlerin %95’ini gece görüşünü işleyen çubuk hücreleri oluşturur. Koniler ise renkli görüntüyü işler. Bu hücreler, gelen ışığı fotonlar olarak taşır ve onları kimyasal sinyallere dönüştürür. En iç tabaka; aksonları (nöronların uzantıları) beyine kadar uzanan küçük nöronlardan oluşan RGC’den oluşur. Fotoreseptör hücreler tarafından toplanan görsel bilgiyi taşırlar ve beyne elektriksel uyaranlar olarak yollarlar. RPE hücreleri tek tabakalı, hekzagonal ve çok pigmentli hücrelerdir.
Retinal Dejeneratif Hastalıklar
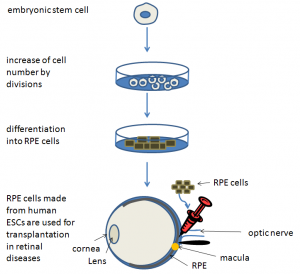 Retinitis Pigmentosa (RR) ve yaşa bağlı makular dejenerasyon (AMD) gibi retinal dejeneratif hastalıklar, retinal fotoreseptörlerin erken kaybı ve RPE’den kaynaklıdır. RP’nin ana belirtileri gece körlüğü ve görüşte sürekli azalmadır. Bu durum çoğu hastada erken yaşta başlayarak en sonunda körlükle sonuçlanır. AMD öncelikle merkezi görüşün kaybına neden olur. WHO tarafından yapılan çalışma, AMD’ye sahip 170 milyon ve RP 1,5 milyon insanın varlığını rapor eder. AMD en yaygın görme kayıpları arasında üçüncü sıradadır. Günümüzde mevcut olan terapiler sadece hastalığın ilerleyişini geciktirir ve bu ilerlemeyi azaltmak için etkili tedavi edici müdahale konusunda eksiklik vardır. İnsan iPSC türevli retinal kök hücre aktarımı, tedavisi olmayan bu hastalıklar için potansiyel bir tedavi yöntemi olabilir.
Retinitis Pigmentosa (RR) ve yaşa bağlı makular dejenerasyon (AMD) gibi retinal dejeneratif hastalıklar, retinal fotoreseptörlerin erken kaybı ve RPE’den kaynaklıdır. RP’nin ana belirtileri gece körlüğü ve görüşte sürekli azalmadır. Bu durum çoğu hastada erken yaşta başlayarak en sonunda körlükle sonuçlanır. AMD öncelikle merkezi görüşün kaybına neden olur. WHO tarafından yapılan çalışma, AMD’ye sahip 170 milyon ve RP 1,5 milyon insanın varlığını rapor eder. AMD en yaygın görme kayıpları arasında üçüncü sıradadır. Günümüzde mevcut olan terapiler sadece hastalığın ilerleyişini geciktirir ve bu ilerlemeyi azaltmak için etkili tedavi edici müdahale konusunda eksiklik vardır. İnsan iPSC türevli retinal kök hücre aktarımı, tedavisi olmayan bu hastalıklar için potansiyel bir tedavi yöntemi olabilir.
Kök Hücre Temelli Terapötik Yaklaşım
Dünyada birkaç grup tarafından, başarılı hücre tedavisi yöntemleri deneysel düzeyde yapıldı. Bu strateji, uyarılmış pluripotent kök hücre teknolojisindeki gelişmelerle mümkün oldu. Bu hücreler vücuttaki herhangi bir hücre türünü üretme potansiyeline sahiptiler. iPSC, embriyonik kök hücrelere karşı avantajlıydı çünkü hastaya özgü olarak yapılabiliyordu. Bu sayede kalıtsal hastalıklar laboratuvar ortamında iPSC temelli modellerle çalışılabiliyordu. Takashi ve arkadaşları tarafından yapılan bir çalışmada RPE’nin başarılı transplantasyonu küçük bir hasta grubunda görüşü düzeltti.
Retinal hücrelerin yenilenme kapasitesi azdır ve bu nedenle hastalıklar 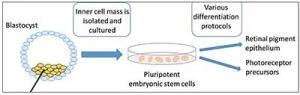 körlükle sonuçlanır. Bu nedenle tedavi edilemeyen göz hastalıkları için bir tedaviye ihtiyaç vardır. Bunun yanı sıra, hastalığın temelindeki mekanizmaları anlamak, tedavi edici stratejileri değerlendirmeden önce kritik rol oynar. Hücreye dayalı stratejiler allojenik (farklı bir insandan alınan hücrenin transplante edilmesi) kök hücre terapisini ve kişisel hücre terapisini içerir.
körlükle sonuçlanır. Bu nedenle tedavi edilemeyen göz hastalıkları için bir tedaviye ihtiyaç vardır. Bunun yanı sıra, hastalığın temelindeki mekanizmaları anlamak, tedavi edici stratejileri değerlendirmeden önce kritik rol oynar. Hücreye dayalı stratejiler allojenik (farklı bir insandan alınan hücrenin transplante edilmesi) kök hücre terapisini ve kişisel hücre terapisini içerir.
iPSC’ten Retinal ve Nöroretinal Kök Hücre Tiplerinin Üretilmesi
Farklılaşmamış kök hücre türleri, istenilen hücre tiplerinin elde edilmesi için bazı faktörlerle muamele edilir. İnsan iPSC işlevi otonomdur. Dinamik, kompleks, spesifik büyüme faktörlerinin, sitokinlerin ve hücreler arası matriks moleküllerinin dahil olduğu mikroçevredeki değişimleri gerektirir. Özel büyüme faktörlerinin ve küçük moleküllerin spesifik kombinasyou ve uygun konsantrasyonları istenilen hücre tipinin elde edilmesinde anahtar rol oynar.
Kemirgen model sistemi, görüş kaybının patogenezi hakkında değerli bilgiler verir. Fakat, kemirgen ve insan sistemi arasındaki klinik farklılıklar sınırlamalar getirir. Alternatif bir strateji, biyopsiyi ya da post-mortem (kadavra) retina dokusunu kullanmayı içerir. Fakat bu alternatifler de hastalığın ilerleyişini gözlemlemek açısından uygun olmayabilir. Diğer bir zorluk ise doku miktarının çok az olmasıdır. Bütün bu zorluklar değerlendirildiğinde, iPSC türevli retinal hücreler var olan sorunları aşabilir. iPSC türevli hücrelerin hastalıkla ilişkili hücre tiplerine farklılaşmasındaki son gelişmeler tıp alanında devrim yarattı. Sadece mutant genin tanımlanması için değil, aynı zamanda erken vakalarda görme kaybının ilerlemesinin gözlemlenmesi ve geriye çevrilmesi için de umut vericidir. iPSC’nin anlayışımıza katkı sağladığı 4 alan:
1) hastalarda hastalık yapıcı mutasyonunun yeni nesil DNA dizileme yöntemiyle tanımlanması,
2) Hastalığa neden olan hücresel ve moleküler mekanizmaların ortaya çıkarılması,
3) görme kaybının ilerlemesinin engellenmesi için küçük moleküllü ilaç denemeleri,
4) gen düzenlenmesiyle allojenik ya da otolog hücre terapisi.
Yeni nesil dizileme yöntemleri; özellikle AMP ve RP gibi kalıtsal retinal hastalıklardan yeni genlerin ve mutasyonların ortaya çıkmasına katkı yapar.
Gen Terapisi
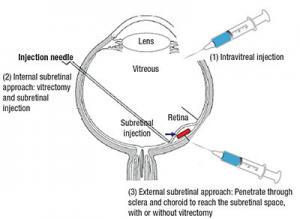 İşlevsel bir proteinin gen terapisi yöntemiyle onarılması, dünya çapında bazı gruplar tarafından tedavi edici bir strateji olarak test edildi. Başarılı bir çalışmada, RP hastaları için viral vektör yoluyla MFRP proteini aktarıldı. MFRP’nin aktarılması sonucu hücre iskeleti onarıldı. Aynı yöntemi farede de test edip, görsel iyileşme gözlemlediler. 2014 yılında yapılan başka bir çalışmada CEP-290 proteini aktarıldı. CEP-290 genindeki mutasyonunun fotoreseptör kaybına neden olduğu biliniyor.
İşlevsel bir proteinin gen terapisi yöntemiyle onarılması, dünya çapında bazı gruplar tarafından tedavi edici bir strateji olarak test edildi. Başarılı bir çalışmada, RP hastaları için viral vektör yoluyla MFRP proteini aktarıldı. MFRP’nin aktarılması sonucu hücre iskeleti onarıldı. Aynı yöntemi farede de test edip, görsel iyileşme gözlemlediler. 2014 yılında yapılan başka bir çalışmada CEP-290 proteini aktarıldı. CEP-290 genindeki mutasyonunun fotoreseptör kaybına neden olduğu biliniyor.
Uygulamada Zorluklar
Başarılı bir şekilde üretilen RPE ve fotoreseptörlerin klinik çalışmalara başarılı bir şekilde aktarılabilmesi için bazı zorluklar mevcuttur. Bunlar;
1-Aktarım türü: En büyük zorluk hücreleri aktarmada standart bir yöntem oluşturmak ve bu enjeksiyonları yapabilmeleri için klinisyenleri eğitmektir. Anahtar noktalar; depolama koşulları, dondurma-çözme etkinliği, hücrenin çözünürlüğü ve kullanılacak cerrahi aletin türü tedavinin etkinliğinie etkileyecektir. Maksimum etkinlik için tüm bu değişkenlerin optimize edilmesi gerekir.
2-Hücrelerin hayatta kalımı: Aktarıldıktan sonra hücrelerin hayatta kalması çoğunlukla yaşa ve hastalığın aşamasına bağlıdır. Ayrıca hücrelerin canlılığı, saflığı ve türü de faktörler arasındadır.
3-Hücrenin ortama uyum sağlaması: Transplante edilen hücrelerden ne kadarının görme işlevine katıldığı önemlidir. Yapılan bazı çalışmalarda dış zarı enzimlerle zayıflatarak hücrelerin retinaya ulaşması deneniyor.
4-Bağışıklık sistemi cevabı: Hücreler retinaya ulaştığında, bağışıklık sistemi tepkisinin hedefi olurlar. Bağışıklık sistemi zayıflatılmış hayvan modellerindeki terapiler, hücrelerin uzun süre hayatta kalmasına yardım eder. Maymunların bağışıklık sistemi, sıçanlar gibi küçük yapılı canlılara kıyasla insanlara daha çok benzer. Küçük yapılı canlılarla çalışmak da yararlı bilgiler sağlarken, iPSC türevli terapilerin kliniğe aktarılabilmesi için büyük yapılı canlılar daha yararlıdır.
5-Hücrelerin işlevsel olarak entegre olması: Nöral ağa hücrelerin işlevsel olarak entegre olması, transplante olan hücrelerin etkinliğine bağlıdır. Hücreleri büyüme faktörleri ile birlikte enjekte etmek, hücrelerin daha yüksek oranda hayatta kalmasına ve böylece daha iyi işlevsel entegrasyon sağlamasına yardım edebilir.
PR transplantasyon deneylerinin klinik öncesi çalışmalarda görsel işlevleri onardığı görüldü. Buna ek olarak, tümör oluşumu ve istenmeyen farklılaşmalar olabilir. Bu nedenle iPSC türevli hücre terapileri güvenliği hala test edilmektedir. Var olan teknik sorunlar aşıldığında iPSC hücre terapisi yöntemi, tedavi edilemeyen körlük vakaları için kullanılabilir.
Kaynakça:
Rathod ve ark. Induced pluripotent stem cells (iPSC)- derived retinal cells in disease modeling and regenerative medicine. Journal of Chemical Neuroanatomy https://doi.org/10.1016/j.jchemneu.2018.02.002
Yazar: Ayça Olcay
