Canlılar hücrelerden oluşur. Hücrelerin yapısında da organik ve inorganik bileşikler yer alır. Yapısında karbon, hidrojen ve oksijen atomları birlikte bulunan ve canlı hücrelerde sentezlenen moleküller organiktir. Bu atomlardan en az bir tanesine sahip olmayan, canlı vücudunda sentezlenemeyen, dışarıdan alınan bileşikler inorganiktir. Genellikle C (karbon atomu) içermezler. Formülü CH4 olan metanı örnek verebileceğimiz hidrokarbonlar oksijene sahip olmadığı halde organik moleküller grubuna dahildir.
Canlıların yapısında bulunan inorganik bileşikler şunlardır:
*Su
*Mineraller
*Asitler
*Bazlar
*Tuzlar
İnorganik Bileşiklerin Genel Özellik ve Görevleri Nelerdir?
İnorganik bileşikler öncelikle organik bileşiklerle birlikte hücre yapısına katılır. Metabolik faaliyetleri düzenleme görevi olan inorganik bileşikler yıpranmış dokuların onarımına da yardım eder. Vücuda dışarıdan hazır alınan bu bileşikler sindirime uğramaz, dolayısıyla hücre zarından içeri doğrudan geçebilir. Organik bileşikler enerji verse de inorganik bileşiklerden hücre solunumunda enerji elde edilemez. Ancak kemosentez yapan canlılarda demir, amonyak, hidrojen gazı, sülfür, hidrojen sülfür, nitrit gibi inorganik moleküllerden kimyasal enerji elde edilebilmektedir. Bazı mineraller yardımcı yani kofaktör olarak enzimlerin yapısına katılır. İnorganik bileşiklerin kanın osmotik basıncını ayarlama görevi de bulunur.
Su Yaşamsal Önemdedir
İnorganik bileşiklerden biri olan su yaşamsal öneme sahiptir. Organizmalardaki su oranı genellikle % 70 oranındadır. Su bitkileri % 98 oranında su içerebilir. Bitki tohumlarında bu oran % 5 ile 15 arasındadır. İnsan vücudundaki su oranı yaklaşık %65’tir. Ancak her doku aynı oranda su içermez. Kemiklerdeki su oranı % 20 iken beyin hücreleri % 85 oranında su içerir. Yaşlanmayla birlikte bu oranlar azalmaktadır.
Kapalı formülü H2O olan bir su molekülü formülden de anlaşılacağı gibi iki tane hidrojen ile bir tane oksijen atomuna sahiptir. Polar kovalent bağlar taşıyan su iyi bir düzenleyici, çözücü ve madde taşıyıcıdır. Hücrelerdeki yaşamsal faaliyetlerin, kimyasal tepkimelerin devam edebilmesi ve enzimlerin çalışabilmesi ortamda yeterince su bulunmasına bağlıdır. Bu nedenle yaşam susuz devam edemez. Besinlerin sindirilebilmesi için de su gereklidir. İnsanlar yiyecek olmadan haftalar boyunca yaşayabilse de su olmadan birkaç günden fazla yaşayamaz.
Terleme ile su kaybedilir ve bu mekanizması ile vücut ısısı düzenlenir. Solunum, idrar ve dışkılama yoluyla da insan vücudundan sürekli su kaybı gerçekleşir. Bu nedenle kaybedilen su yerine koyulmalıdır. Sağlıklı bir yaşamın devam edebilmesi için günlük ortalama su tüketimi 1,5 – 2 litre olmalıdır. Su bitkiler için de çok önemlidir. Su, besin ve oksijen üretimini sağlayan fotosentez olayında kullanılır. Otsu bitkilerin bulundukları ortamda dik durabilmelerini sağlayan da sudur. Su, bir hücreli canlıların çoğu için genel yaşama ortamıdır.
İnsan Vücudundaki Mineraller
İnsan vücudundaki hücrelerde demir, kalsiyum, fosfor, sodyum, potasyum, magnezyum, iyot, flor gibi birçok mineral bulunur. Örneğin 70 kilogram ağırlığındaki bir insanın vücudunda bulunan ortalama mineral miktarı 3 kilogramdır. Vücudun bazı minerallere ( demir, iyot, bakır, manganez, çinko) ihtiyacı daha az, bazılarına ( klor, sodyum, potasyum, kalsiyum, magnezyum, fosfor ) ise ihtiyacı daha çoktur.
İnsan vücudunda en çok rastlanan, diş ve kemiklerin yapısında yer alan mineral Ca sembolü ile gösterilen kalsiyumdur. Mineraller suda erimiş olarak ya da dışarıdan alınan besinlerle vücuda girer ve sindirilmeden doğrudan kana karışır. Mineraller düzenleyicidir, vücuttaki hormon, vitamin, enzim gibi önemli moleküllerin yapısına katılır ancak enerji verme özelliğine sahip değildir. Bir mineralin eksikliğini başka bir mineral gideremez. Mineraller gerektiğinden fazla alınırsa vücuda zarar verebilir. Mineraller hücrelerde ya tuz şeklinde bulunur ya da yağ, karbonhidrat ve protein gibi bazı organik bileşiklere bağlı olarak bulunur. Mineraller vücuttaki iyon dengesini de sağlar. Terleme, dışkılama, idrar yoluyla mineral kaybı olacağından düzenli olarak besinlerle alınmalıdır. Fazla terleyen, fazla idrar çıkaran, fırın gibi ortamlarda çalışan kişilerde mineral kaybı normalin üzerindedir. Bu kişiler yeterince su içmeli ve kaybedilen mineralleri yerine koymalıdır.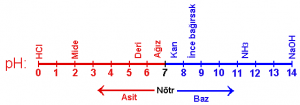
Asitlerin Yapısı ve Görevleri
İnorganik bileşiklerden biri olan asitler suda çözündüğü zaman ortama H+ ( hidrojen iyonu) verir. Ekşi tatları asitlerin karakteristiğidir ancak asitler aynı zamanda yakıcı olduğundan bilinmeyen bir maddenin ne olduğunu anlamak için tadına bakmak tehlikeli olabilir. Günlük hayatımızda mutfaklarda sık kullanılan sirke ve limon asidik yapıdadır. Midemizde de protein sindirimine yardımcı olan seyreltik HCl (hidroklorik asit) salgılanır. Mide asidi artarsa yakıcılığı nedeniyle ülser gelişir. Asitlerin pH değeri 0–7 arasındadır. Asitlerin bir diğer özelliği de içine batırılan mavi turnusol kağıdının rengini kırmızıya çevirmesidir. Bazı asitler ayıraç (indikatör) özelliğindedir. Örneğin nitrik asit proteinin ayıracıdır. Protein varlığında sarı bir renk oluşur. Asitlerin bazıları (sülfürik asit ve hidroklorik asit) inorganik, bazıları da ( yapısında karbon içerenlerin birçoğu) organiktir. Limondaki sitrik asit, sirkedeki asetik asit ile yoğurt ve ayranda bulunan laktik asit organik asitlere örnektir.
Bazların Yapısı ve Görevleri
Bazlar suda çözünürse ortama OH- (hidroksit iyonu) verir. Tatları acı olup dokunulduğunda sabunda olduğu gibi ellerde kayganlık hissi bırakır. Bazik bir çözeltiye batırılan kırmızı turnusol kağıdının rengi maviye döner. Bazların pH değerleri 7–14 arasındadır. Kalsiyum hidroksit, potasyum hidroksit, baryum hidroksit ve sodyum hidroksit gibi inorganik bazlar hem nem hem karbondioksit tutar. Dolayısıyla bu bazlar karbondioksidin ayıracıdır. Bazların çoğu inorganik olsa da yapılarında azot ve karbon bulunan organik bazlar da vardır. Yönetici moleküller olan nükleik asitlerin yapısındaki adenin, timin, sitozin, guanin ve urasil bazları organiktir.
Vücuttaki pH Değişimlerinin Önemi
Bir çözeltinin asidik mi yoksa bazik mi olduğunu belirleyen içeriğinde bulunan serbest hidrojen iyonlarının (H+) derişimidir. Hidrojen iyonlarının derişimi ise pH değerleriyle ifade edilmektedir. Bir çözeltinin pH değerinin 7 olması o çözeltinin nötr olması anlamına gelir. Nötr çözeltilerde OH- ( hidroksit) ve H+ ( hidrojen) iyonları eşit yoğunluktadır. Bir çözeltinin pH’ı 7’nin altındaysa asidik, 7’nin üzerindeyse bazik yapıdadır. Çözeltilerde asitlik artarsa hidrojen iyonları, bazlık artarsa hidroksit iyonları artar. Canlı hücrelerdeki ve kandaki pH değerlerinin küçük değişimleri bile yaşamsal tehlike yaratabilir. İnsan kanının normal pH değerinin 7,4 olduğu bilinir. Bu değerin 7’ye inmesi veya 7,8’e yükselmesi durumunda her ne kadar düzenleyici mekanizmalar devreye girse de düzenlemenin gerçekleşemediği durumlarda canlı kısa sürede yaşamını kaybedebilir.
Asit-Baz Dengesi Bozulursa Neler Olur?![Canlıların Yapısındaki İnorganik Bileşikler]()
İnsan vücudundaki asit-baz dengesinin bozulması bazı sorunlara yol açabilir çünkü biyokimyasal tepkimeler ancak belirli pH değerlerinde gerçekleşir. Sinirsel kökenli ağrılar, depresyon, dişlerde çürüme, saçlarda dökülme, kalp krizi geçirme, kronik yorgunluklar, konsantrasyon eksiklikleri ortaya çıkabilecek sorunlardan bazılarıdır. Her bitki türünün pH ihtiyacı farklıdır. Mesela çam ağaçları ve biber asit karakterli, akasya ağaçları da bazik karakterli toprakları sever. Topraktaki asit-baz dengesizlikleri bitkileri çeşitli şekillerde etkiler. Ortanca bitkisinin çiçek rengi toprağın pH değerinden etkilenir. Kireçli (pH değeri 6–6,2 arasında olan) topraklarda ortancaların çiçekleri pembe-beyaz, pH değeri 5,2–5,5 arasında olan asit topraklarda ise mavi-mor renkte açar. Örneğin çiçekleri pembe renkli bir ortanca bitkisinden elde edilen fide başka bir bahçeye ekildiğinde mavi renkli çiçeklerle karşılaşılabilir. Bunun nedeni pH değişiminin genlerin işleyişini değiştirmesidir. Kalıtım biliminde geçici olan bu tür değişimlere modifikasyon adı verilir.
Tuzların Yapısı ve Görevleri
Asit ve bazların birlikte tepkimeye gitmesiyle tuz denilen nötr bileşikler oluşur. Asitteki H+ iyonuyla bazdaki OH- iyonu birleşince su molekülü oluşur. Geriye kalan iyonlar da birleşerek tuzları oluşturur. En önemli tuzlar potasyum, magnezyum, kalsiyum ve sodyum tuzlarıdır. En bilinen ve günlük hayatta çok kullanılan tuz ise sodyum klorür (NaCl) yani sofra tuzudur. Bu tuzda bulunan sodyum ve klor iyonları vücuttaki çeşitli sıvıların osmotik basıncını düzenler. Ancak fazla tuz tüketimi kan basıncını yükseltir, böbrek ve kalp hastalıklarına zemin hazırlar. Tuzlar bulundukları ortamların pH’ını değiştiremez, turnusol kâğıdında değişiklik yapamaz.
İyon İhtiyacının Karşılanması![Canlıların Yapısındaki İnorganik Bileşikler]()
İnsanlarda sinirsel iletimin ( elektriksel iletimin)ve daha başka faaliyetlerin gerçekleşebilmesi için iyonlara ihtiyaç vardır. Tuz, baz ve asitler suda iyonlarına ayrılarak vücudun çeşitli iyon ihtiyacını karşılar. İyonlar suda çözünerek hücre dışına ya da içine taşınır. Canlı yaşamının devamı hücrelerdeki ya da hücreler arasındaki sıvıların içerdiği iyon dengesine bağlıdır.
Kaynakça:
http://www.biyolojiportali.com
http://www.biyolojisitesi.net
Yazar: Müşerref Özdaş


